海水魚の浸透圧調整物質は水中で水素結合しない? – 分子シミュレーションと実験から探る
海水魚の浸透圧調節物質とは?
海水は3.5%程度の塩分を含んでおり、その濃度は一般的な生物の体液(たとえば人体では0.9%)よりも高いため、海水中に生物の細胞が存在すると、そのままでは塩が野菜に浸透して漬物ができるように、塩分が細胞内に侵入して生体機能を阻害してしまいます。
そこで海水魚は、食物として摂取したアミノ酸を分解する際に得られる尿素を高濃度に保持することで、細胞内への塩分の侵入を防いでいます。このように、浸透圧を調節する役割を持つ分子を浸透圧調節物質と呼びます。さらに尿素には、タンパク質を不安定化させる働きもあります。そのため海水魚は、尿素と同じく浸透圧調節物質であり、タンパク質を安定化させる働きを持つトリメチルアミンオキサイド(TMAO)を同時に用いることで、塩分の侵入を防ぎつつ、タンパク質の働きも維持しているのです。
サメをはじめとした海水魚の生体細胞内では、TMAOと尿素が1:2という適切な割合で共存することが知られており、この2つの分子は互いに結合すると思われてきました。個々の分子はタンパク質と相互作用して安定化か不安定化をもたらしますが、TMAOと尿素が結合したものはタンパク質と相互作用しません。そのため、タンパク質に対するTMAOと尿素の反対の効果は、両者が結合することで打ち消しあうと思われてきました。しかし一部の研究では、TMAOと尿素は水素結合を形成しないことも指摘されていました。

高精度分子シミュレーションで追う分子の動きと安定構造
TMAOと尿素は水素結合を形成するのでしょうか? この謎を解くため、水に溶かしたTMAOと尿素の分子間相互作用を理論と実験の両方を用いて調べました。しかし水中の分子は非常に早く動くため、その結合状態を調べることは非常に困難であるという問題があります。そこで、はじめに高精度のコンピューターシミュレーションを用いて、水中のTMAOと尿素がどのように結合するかを調べました。
用いた手法は全原子分子動力学法と呼ばれ、ニュートン方程式に従って原子の位置を時間発展させることで、分子の動きを追うことができる手法です。原子に働く力を計算するために経験的パラメータを用いた古典分子動力学法(古典MD)が広く用いられていますが、今回はシュレディンガー方程式を解いて原子に働く力を計算する第一原理分子動力学法(ab initio molecular dynamics, AIMD)を水中のTMAOと尿素に初めて適用しました。計算コストが非常に大きいため、スーパーコンピューターを用いた膨大な量の計算が必要となりました。計算の結果、図に示すように、AIMDではこれまでの理解と反し、TMAOと尿素が直接水素結合する構造は不安定であるという結果が得られました。
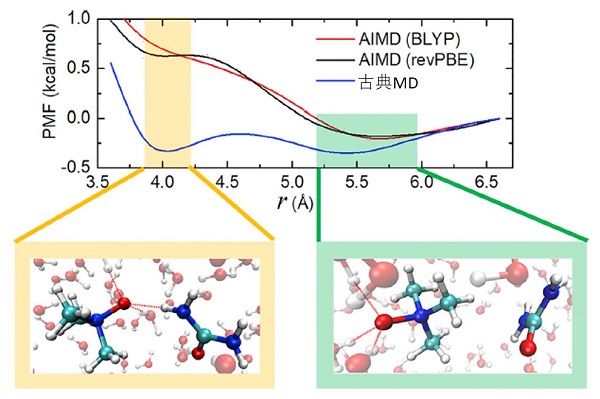
横軸はTMAOの酸素と尿素の炭素原子の距離。縦軸はエネルギーで、エネルギーが小さい方が安定であることを示す。黄色はTMAOと尿素が直接水素結合する領域、緑は間に水分子を介して結合する領域である。古典分子動力学法(古典MD)は直接的な水素結合が安定であるという結果となるが、第一原理分子動力学法(AIMD)ではそれが不安定であるという結果となる。
TMAOと尿素は直接水素結合しない – 理論と実験の比較で実証
理論的な発見を裏付けるため、赤外分光と核磁気共鳴分光を用いた測定を行い、理論計算の結果と比較したところ、計測とシミュレーションの一致から、TMAOと尿素はこれまでの理解と反対に、水中で直接的な水素結合を形成しないことがわかりました。これは、TMAOの酸素原子は尿素の水素原子よりも水分子の水素原子と結合することを好むためです。したがって、TMAOの酸素原子は水分子によって占有されるため、尿素は水素結合によってTMAOと結び付くことができません。
しかし、2つの分子は細胞内のタンパク質を守るために互いに結合することが知られています。そこで本研究では、尿素はTMAOの酸素原子ではなく疎水部と結合することを明らかにしました。つまり、海水魚の細胞内に存在するTMAOと尿素がタンパク質の周囲で共存したとき、両者が水素結合により強固に結合してタンパク質への作用を失うのではなく、タンパク質の安定化・不安定化のバランスを保ちながら海水中でタンパク質の機能を維持していることがわかりました。
生体機能維持の分子レベルでの解明を目指して
本研究成果により水中でのTMAOと尿素の相互作用に関する分子レベルの理解が得られたことは、これら2つの分子の化学的なシャペロン(タンパク質の機能を維持するための補助剤)としての役割を理解するための鍵となります。合成生物学の観点からは、こうした基礎的な理解によって人工シャペロンの開発が進み、次世代の医療への貢献が期待されます。
また、水深6000メートルよりも深い「超深海」においては、TMAOと尿素に加えて「糖類」が介在することで、非常に高い水圧の中でも酵素の働きが保たれているのではないかといわれはじめています。今後は、分子シミュレーションで取り扱う分子の範囲を糖類などへも広げることで、そのような過酷な環境でタンパク質の機能が保たれる仕組みを明らかにし、生体機能維持のための基礎学理を深めていきたいと考えています。
参考文献
この記事を書いた人

-
大戸達彦(写真左)
大阪大学大学院基礎工学研究科助教。2013年東京大学大学院化学システム工学専攻博士課程修了。博士(工学)。日本学術振興会特別研究員(PD)を経て、2013年より現職。専門は計算物理・量子化学計算。特に経験的パラメータを必要としない第一原理計算を用いて、振動分光スペクトル、ナノスケールの電気伝導度の計算などに取り組んでいる。その他の研究についてはWebサイトを参照のこと。
水上渉(写真中)
九州大学総合理工学研究院助教。2011年総合研究大学院大学機能分子科学専攻博士課程修了。博士(理学)。Marie Curie Research Fellow、 理化学研究所基礎科学特別研究員を経て、2015年より現職。専門は分子に対する電子状態理論および振動状態理論。量子化学理論・プログラムの開発や、波動関数理論に基づく定量的な分子分光シミュレーションを中心とした研究をおこなっている。
永田勇樹(写真右)
マックスプランク・ポリマー研究所グループリーダー。博士(理学)。2007年京都大学大学院理学研究科博士課程修了。同年、ドイツBASF社に勤務。2009年からカリフォルニア大学アーバイン校博士研究員。2011年にドイツに戻り現職。2016年より分子科学研究所客員准教授兼任。主な研究分野は理論化学、分子分光、界面科学。趣味は囲碁、列車旅行。




