緑内障による失明を食い止めたい – 個別化医療への挑戦
【関連記事】AIによる緑内障の自動診断 – 未来型の個別化医療を目指して
緑内障とは
緑内障は目と脳を繋ぐ視神経が障害を受け、視野が少しずつ見えなくなっていく病気です。40 歳以上の約 5%、70 歳以上では 10%以上が罹患し、現在失明原因の第一位の眼疾患となっています。人口の高齢化に伴い、本邦では緑内障による失明患者数が毎年増加しています。
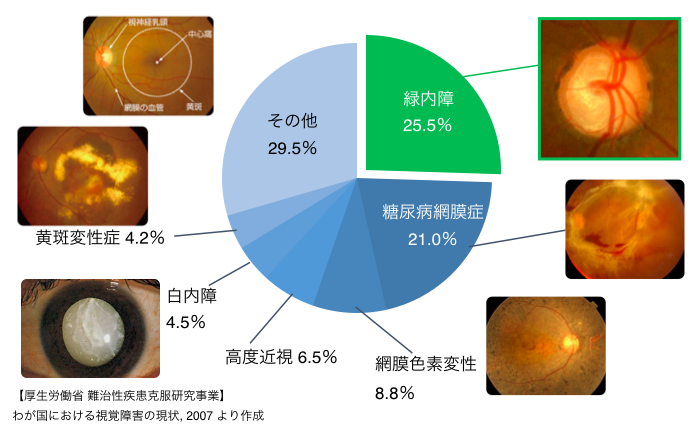
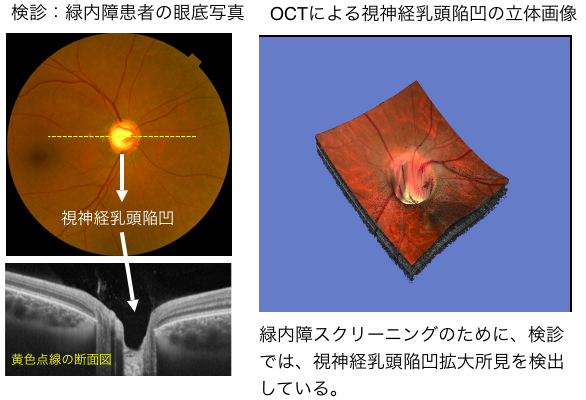
緑内障は、自覚症状で気づきづらい病気です。そのために、患者自身が病気を疑って眼科に来院することはほとんどありません。主には、検診やコンタクトレンズやメガネを作成する際に、偶然見つかることが大半であり、早期発見のためには検診を受けることが重要です。緑内障は眼底検査で視神経乳頭陥凹という特徴的な所見を契機に緑内障を疑われ、視神経乳頭の神経障害部位と視野欠損部位が一致し、脳や目の別の病気を認めていないときに診断されます。検診では、主には眼底写真により視神経乳頭陥凹の拡大所見がみられる場合に、緑内障疑いとして、精密検査に回っていただくことになっております。
緑内障の治療としては、眼圧下降が唯一証明されている有効な治療法です。現在では、20種類を超える眼圧下降点眼薬の中からまず一剤を使用し、目標値まで眼圧を下降させます。日本人の正常者の平均眼圧は14 mmHgであり、緑内障の視野障害の程度に従って、一般的には、初期緑内障では19 mmHg、中期では16 mmHg、後期では14 mmHgを目指します。緑内障と聞くと、眼圧が高いイメージがあるかもしれませんが、本邦では、眼圧が正常範囲内の正常眼圧緑内障が大半で、無治療時の眼圧を複数回測定して平均値を求め、治療によりその値の20~30%の眼圧下降を目標とします。点眼後まもなく眼圧下降が得られるので、目標の眼圧が得られるまで、複数の点眼薬を併用しながら対応します。しかし、点眼薬で目標の眼圧にまで眼圧下降を得られない場合には、レーザー治療や外科的治療を行って眼圧下降を行います。視野障害が進行しているか否かを評価するには、定期的に3〜6ヶ月おきに視野検査を行い、複数回の測定結果から視野障害の進行を判定します。進行と判定される場合には、さらに追加の点眼を行い、手術を計画することもあります。
緑内障による失明患者の増加
先に述べました通り、緑内障による失明患者数は毎年増加しています。その原因には、(1) 高齢者人口の増加、(2) 一度失われた神経は回復しない不可逆性、(3) 現在の治療の限界などが考えられています。
(1) 加齢が緑内障の危険因子であり、高齢者人口が増えると緑内障患者は増加します。
(2) 緑内障の不可逆性障害については、早期発見・早期治療が奏功します。最近我々の施設では、前視野緑内障という病期に注目しています。緑内障では、まず視神経乳頭陥凹の拡大が見られ、同時に網膜神経線維の欠損が見られます。これらの障害はゆっくりと進行するために、障害が軽度の場合には、まだ視野障害が検出されない時期があります。これが前視野緑内障です。視神経や網膜神経線維の障害部位と視野異常の部位が一致すること、また視野異常が慢性に進行することが緑内障の定義です。前視野緑内障は視野異常がないため、緑内障として治療にあたるのかコンセンサスがありませんでした。我々は前視野緑内障患者の前向き研究を行っており、視野進行の危険因子の検討を行っております。16ヶ月の経過で約13%が緑内障に移行することが判明しました。緑内障による視野障害のスピードは非常にゆっくりではありますが、緑内障で障害される網膜神経節細胞は加齢現象でも減少します。つまり、現状の治療が奏功していても、徐々に視野障害が悪化することが多くあります。寿命を全うするまでに日常困らない視覚を保持することが、緑内障治療の最終的な目標ですので、早期発見・早期治療の意味から、前視野緑内障とどう向き合うのかが重要です。しかし、前視野緑内障の診断は施設によって発見率が異なります。今後は眼底写真や光干渉断層計(Optical coherence tomography; OCT)検査による自動診断による診断の標準化が行われる必要があります。
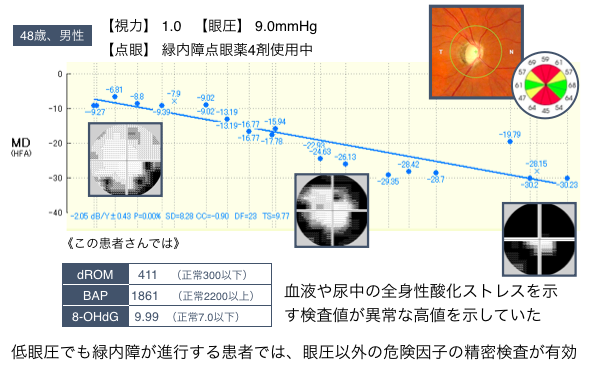
(3) 続いて、現状の治療法の限界に関してまとめます。緑内障では、古くから眼圧による視神経の障害が重要な病因のひとつとされ、主に眼圧下降治療が行われています。現状、薬剤、手術などはすべて眼圧下降を目的とした治療です。しかし、我々の後ろ向き研究では、眼圧下降治療に反応しない患者が約4割も存在していました。緑内障は多因子疾患で、眼圧以外の要素が緑内障の進行に悪影響を与えているからです。眼圧に終始した現在の治療体系も、緑内障失明患者が増加している一因と考えられます。こうして、緑内障による失明が増加しているのは、治療開始時期が遅く、その治療自体も有効でない症例が未だ多く存在することが問題と考えられます。実際に、東北大学の眼科外来では、「眼圧が低いのに進行する緑内障患者」が全国から紹介されてきます。その多くは循環障害や酸化ストレスが異常な高値を示しており、眼圧以外にも明らかな危険因子を有していることが多いのが現状です。
緑内障の危険因子
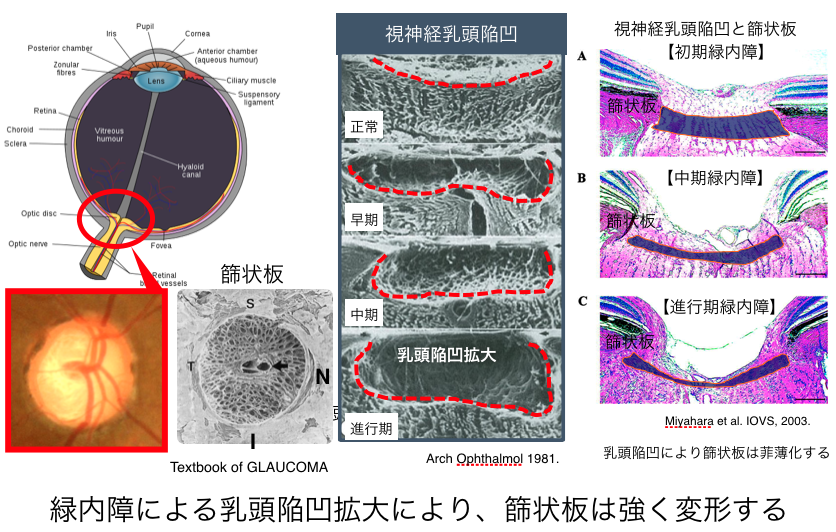
緑内障の原因は、視神経乳頭の深い位置にある篩状板と呼ばれる篩の目の構造組織の部位において異常が出ることが病態と考えられています。この篩の目(篩状板孔)の一つひとつに網膜神経節細胞の軸索が束になって通過しており、視神経乳頭の陥凹拡大により、篩状板の変形や菲薄化、部分的な欠損などが起こり、軸索が絞扼障害され、網膜神経節細胞の細胞死が起こします。
この緑内障進行に影響を与えるのが、緑内障危険因子です。緑内障危険因子として最もエビデンスがあるのが高眼圧です。本邦では、前述のように正常眼圧緑内障が大半ですが、正常域の眼圧であっても、その一日の変動幅が緑内障進行に悪影響を与えるという報告もあります。次いで、眼の血流不全があります。緑内障眼では、視神経乳頭の毛細血管が退縮しており、最近我々のグループから視野異常を呈するより以前の前視野緑内障でも、循環不全が起きていることが証明されています。さらには全身の循環障害や低酸素、酸化ストレスが高値になる状態が緑内障を進行させます。この点は、全国的にも未だあまり注目されておらず、低血圧や高血圧の過剰治療による低血圧、血管攣縮、心臓の病気、貧血や慢性閉塞性肺疾患(COPD)のような肺の疾患、更に頻度が多いのは睡眠時無呼吸症候群などに注意が必要です。全身の血液循環が悪い状態は、当然眼でも循環状態が悪くなり緑内障が悪化します。こうして、眼圧は容易に測定できるため治療開発が進み、現在も点眼液や手術などすべて眼圧下降が治療の中心となっています。しかし、眼圧以外の循環障害や酸化ストレスといった危険因子については、現在、測定方法やその治療意義を調査している最中であり、緑内障の進行を止める方法としては限られているのが現状です。
緑内障個別化医療の足掛かり
ここまでご紹介しましたように、多因子疾患である緑内障を余すところなく治療するためには、各患者さんの病態に基づいた治療が理想的です。眼圧以外の危険因子が緑内障に与える悪影響が大きい場合、現状の眼圧下降治療だけでは緑内障の進行を食い止めることが困難です。カナダのNicolela らの研究グループは、臨床背景を異にする4つの視神経乳頭形状の分類方法を提案しました。
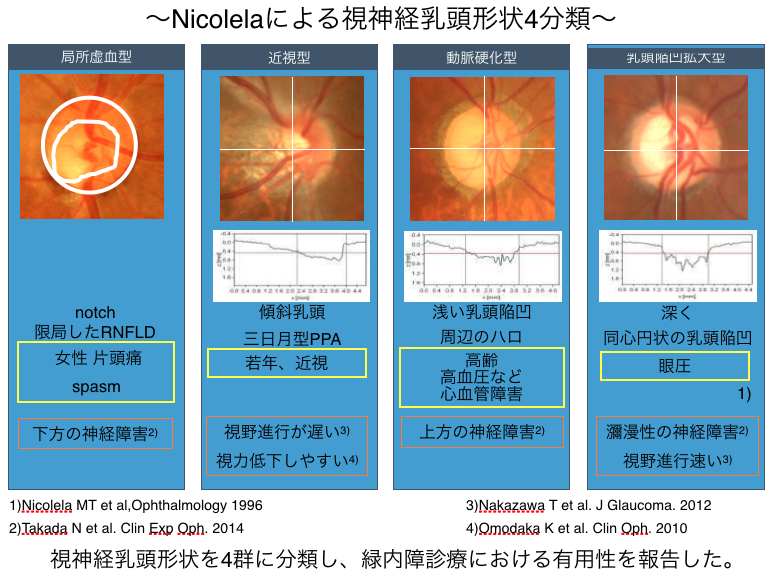
スパスム(血管の攣縮)、近視、血流障害、高眼圧を反映した 4つのグループに緑内障を分類することで、緑内障病態の細分化の足掛かりになり、治療の効率化が図れます。我々の研究グループもこの分類方法に着目して、緑内障診療での有用性について検討を重ねてきました。その結果、眼圧下降治療の効果が弱く進行の早いグループや、緑内障により視力低下する患者の頻度が多いグループ、日常生活の質を維持するのに重要な下方の視野が障害されやすいグループなど、グループ間に診療上注意するポイントに特徴があることが分かったのです。緑内障は多因子疾患であるが故に、病態ごとの細分化により、診療の質が上がってきます。しかし、この分類方法は、眼底写真による肉眼的な画像判定で行われていることから、検者の熟練を要し、一般の診療所では分類が難しいことが問題でした。
今後の展望
眼底を3次元撮影可能なスウェプトソースOCTは高速・高進達性で優れており、日本が世界をリードしています。我々はトプコン社のOCT装置で計測された視神経乳頭部の断層画像を定量化し、自動で緑内障の危険因子の4分類を行うソフトウエアを開発しました。多様な緑内障診療において、病態の細分化や治療の個別化につながる重要な研究です。すべてが自動で緑内障の細分化が可能となれば、将来的には検診センターを含め、全国どこの病院でも標準化された緑内障病態の細分化や治療の個別化につながることが期待できます。現在は眼科医が減少し、地方では眼科医が不在の地域が増えてきています。今後はネットワーク環境を応用した遠隔診療や人工知能による自動診断の補助を受けながら、病態に即した適切な治療体系を組み上げていく必要があります。社会的な重要性の高い緑内障に対しては、眼科医全体としてビックデータを集めることにより、初診時の画像データやゲノム・メタボローム・自己抗体などの最先端バイオマーカーを駆使して、予後を予測し先制医療を行うのに適した眼疾患と考えており、我々の施設では着々と準備を進めています。
参考文献
OCT-Based Quantification and Classification of Optic Disc Structure in Glaucoma Patients. Takada N, Omodaka K, Nakazawa T et al. PLoS One. 2016 Aug 24;11(8):e0160226.
【関連記事】
この記事を書いた人
- 1995年東北大学医学部卒業、2002年東北大学大学院医学系研究科博士課修了。医学博士、眼科専門医。米国ハーバード大学眼耳鼻科病院で3年間の博士研究員を経て、2007年東北大学病院眼科講師となる。2011年3月東日本大震災を経験し、被災地における眼科診療や整備の精力的な活動を行った。同年9月東北大学医学系研究科眼科教授となる。「自分にしてほしい最善の医療を低コストで」をテーマに個別化医療の開発に取り組んでいる。本教室の基礎研究部門は常に多職種にオープンであり、工学、薬学、農学のPhDが研究者として仲間となっている。また、眼科領域でも最先端の技術の恩恵に預かれるように、積極的な共同研究を展開し、常に募集している。「失明ゼロ」を目指し、日本から世界へ発信するべく取り組んでいる。
この投稿者の最近の記事
 研究成果2019年5月15日AIによる緑内障の自動診断 – 未来型の個別化医療を目指して
研究成果2019年5月15日AIによる緑内障の自動診断 – 未来型の個別化医療を目指して 研究成果2016年10月5日緑内障による失明を食い止めたい – 個別化医療への挑戦
研究成果2016年10月5日緑内障による失明を食い止めたい – 個別化医療への挑戦



