小豆の赤色の正体とは? – 新たな色素「カテキノピラノシアニジン」の化学構造
食べもののさまざまな色
イチゴ、ブドウ、スイカ、ニンジン、ナス、サツマイモ、ほうれん草……食べもののさまざまな色は、食欲をそそり生活を豊かにします。これらの植物性食品の色素について、赤や紫、黒色はアントシアニン、橙色はカロテノイド、緑色はクロロフィルと聞いたことがある人もいるかもしれません。
なかでも「アントシアニン」は、ポリフェノールの一種として昨今機能性が注目されていますので、みなさんもなじみのある言葉ではないでしょうか。アントシアニンは花色素としても知られ、赤から紫、青色の花の多くはアントシアニンによります。たとえば、チューリップ、アサガオ、ヤグルマギク、ツユクサ、アジサイなどです。
アントシアニンは、アントシアニジンという発色団に糖がひとつ以上結合した化学構造を持った色素の総称です。発色団は、ある特定の波長の光を吸収し、ヒトの目にはそれ以外の波長の光が届いて色として認知されるため、色を持ちます。
私たちは、赤小豆の種皮から新しい色素である「カテキノピラノシアニジンA, B」を見いだしました。これは、分子内に糖を持たない、アントシアニンとはまったく異なる性質を持つ色素で、餡の紫色もこの色素によることがわかりました。

有色豆の種皮色素はアントシアニン
豆にも種皮が赤や紫、黒いものがあります。最近サラダに用いられている赤インゲン、高原の豆として知られる紫花豆、正月に食べる黒豆、これらの色素はすべてアントシアニンです。豆種皮に含まれるアントシアニンの分子構造はとても単純で、発色団にひとつグルコースが結合しています。豆の種類によって発色団のB環部分の酸素の数が異なります。
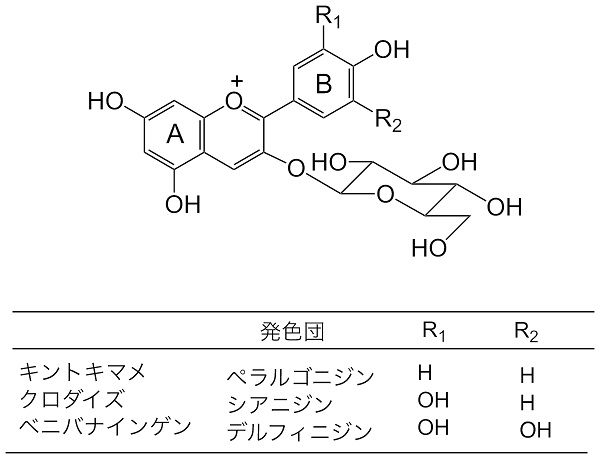
豆種皮のアントシアニン含有量はかなり多く、黒豆では乾燥種皮1gあたり15mg、金時豆でも3mg以上あります。では、小豆はどうなのでしょうか?
小豆といえば赤と思われるかもしれませんが、実は黒、白、斑などさまざまなバリエーションがあります。黒小豆の黒色はアントシアニンであることがすでに報告されていますが、赤小豆に含まれるアントシアニンは極めて微量で、乾燥種皮1gあたりたったの0.0003mg、黒大豆や金時豆の1万分の1以下です。したがって、小豆の赤色はアントシアニンでは説明できません。では、いかなる色素なのだろう? これが、私たちの小豆色素研究の発端、1996年のことです。
紫色色素の発見と色素の単離
種皮色素の研究は、種皮をさまざまな溶媒で抽出し、これを高速液体クロマトグラフィー(HPLC)で分析することから始まります。分析の結果、赤アズキ種皮抽出液には、無色のポリフェノール成分であるプロシアニジン類(カテキンの重合体で、縮合型タンニンともいう)が大量に含まれることがわかりました。一方、赤色物質を見る530nmで検出したクロマトグラムでは、ベースラインの盛り上がりしか観察されず、重合体色素の混合物ではないかと思われました。
ところが、当時一緒に研究していた大学院生が、意図してか間違えてかHPLCの溶出条件を変えたのです。すると、分析時間の終了間際に2本のピークが出現しました。しかも、560nmに吸収極大を示す紫色色素でした。アントシアニンと違ってあまりに脂溶性が高いため、これまでの分析で見逃していたのです。
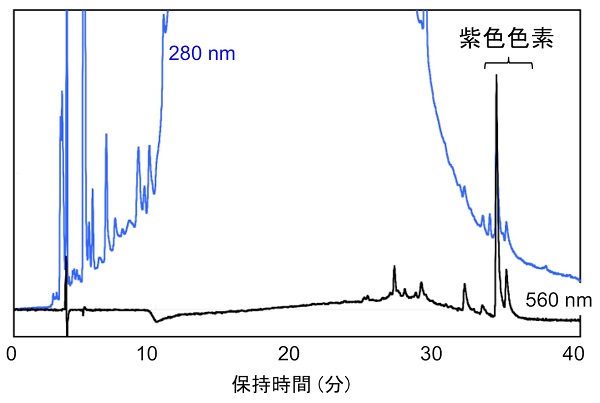
青色の線は280nm、黒色の線は560nmで検出したクロマトグラム。35分付近の2本のピークが紫色色素である。
この紫色色素を標的に単離精製実験を開始しましたが、問題は山積でした。まずひとつ目に、種皮に大量に含まれる無色のプロシアニジン類の除去に苦労しました。そして、色素溶液が室内光でも容易に分解退色してしまうことも実験を困難にしました。最終的に、小豆を吸水させてから数回にわたって温水洗浄し、酢酸エチルで抽出する方法を確立しました。そして、可能な限りの実験を遮光して行いました。たとえば、抽出はステンレス製の寸胴鍋で、濃縮操作は暗幕のなかで、試料は褐色のフラスコに入れてという具合です。そして、数十Kg以上の豆を消費し、私たちは純粋な紫色色素を2種類取り出すことに成功しました。
紫色色素の化学構造
2種類の紫色色素の分子量は、いずれも556で、分子式はC30H20O11と決定しました。現在、純粋に単離できた有機分子の構造は、超伝導磁石を用いた核磁気共鳴スペクトル分析(NMR)、なかでも各種の2次元測定によってほぼ決定できます。しかし、小豆の紫色色素ではそれが成り立ちませんでした。
その最大の理由は、色素分子に四級炭素が多く、水素の数が極端に少ないうえにフェノール性ヒドロキシ基が多数存在したためです。2次元NMRの解析では、水素原子を手がかりに炭素骨格のつながりを決めていくのですが、水素から4結合以上離れるとシグナルが見えません。そのため、部分構造は判明したものの、それらがどう結合しているかを決定できませんでした。
なんとか手がかりが得られないものかとの思いで、光分解物の構造解析を進めることにしました。分解物の分子量は560、分子式はC29H20O12でした。分解物についても多くのNMR測定を行いましたが、完全な構造決定にはさらに誘導体化が必要でした。そして最終的に、分解物の構造情報を元に紫色色素の構造を決定することができました。
決定した化学構造は、シアニジンとカテキンがD環で縮環した新しい骨格の分子であることから、私たちはこの紫色色素を「カテキノピラノシアニジンA, B」と命名しました。
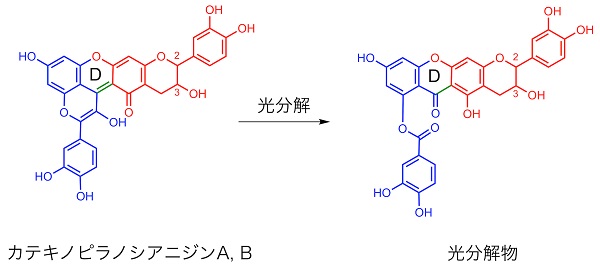
A, Bの違いは2、3位の絶対立体配置の違いによる。いずれも、赤色がカテキン、青色がシアニジン部分(分解物はその変化したもの)を示し、D環で両者が縮環した構造を持つ。
カテキノピラノシアニジンは、水にはまったく溶けず、pHを強酸性から中性まで変化させても紫色のままです。さらに、アントシアニンが退色する弱酸性から中性でもとても安定に色を保つことが明らかになりました。
餡が紫色になる理由
餡にはこし餡と粒餡があります。こし餡は、小豆を煮熟後、渋きりしてから磨砕、裏ごしして種皮を除いてから加糖したものです。少々ざらついた食感がありますが、これは子実体の細胞ひとつひとつが加熱されてばらばらになった餡粒子で構成されているからです。餡粒子は、熱変成した細胞壁・膜の中にα化したデンプンが詰まったもので、大きさは100~200 μmになります。こし餡の紫色は、この餡粒子に種皮色素が吸着して紫色になるものと考えられました。
そこで、加糖前のさらし餡を抽出してHPLCで分析したところ、見事にカテキノピラノシアニジンA, Bが検出されました。さらに、種皮には大量に含まれていたプロシアニジン類が、餡では減っていることもわかりました。これは、製餡工程を考えると実に合理的であると理解できます。渋切りは、水溶性で褐変するプロシアニジン類の除去のために行われ、紫色色素は水に溶けないのですが沸騰水にはわずかに溶けるようで、煮熟中に脂溶性の餡粒子表面に吸着するのです。
小豆が他の豆類とは異なる独特の豆であることは、色素の構造ひとつをとっても明らかといえます。しかし、小豆色素の研究は緒についたばかりで、これから色素の生合成や光分解反応の機構、品種間差や製餡加工における着色など、多面的な研究の展開が必要と考えています。構造が決定できたことは、ゴールではなく研究のスタートラインに立てたということなのです。
参考文献
この記事を書いた人
-
名古屋大学大学院情報学研究科 教授
1982年に名古屋大学大学院農学研究科博士前期課程修了。1992年に同大学院にて博士(農学)の学位を取得。天野製薬(株)研究員、椙山女学園大学生活科学部助手、ドイツコンスタンツ大学客員研究員、名古屋大学大学院人間情報学研究科および情報科学研究科助教授を経て2010年より現職。アントシアニンによる花色発色機構の解明、植物ポリフェノール類の構造、化学合成および機能発現機構に関する研究を行っています。




