神経幹細胞の運命を決定する「Matrin-3」を発見! – タンパク質研究の意義と可能性
神経幹細胞の運命を決定する分子メカニズムとは?
神経幹細胞はさまざまな神経細胞に分化する多分化能と、未分化のまま自己複製する能力とをあわせ持った細胞です。哺乳類の胎生期においては、脳を構成する主要な細胞(ニューロン、アストロサイト、オリゴデンドロサイトなど)に分化することが知られており、それらは複数のシグナル伝達経路や遺伝子、転写因子の特徴的な組み合わせによって調節されています。しかし、これまで神経幹細胞がどのように未分化性を維持するのか、もしくは分化するならどの細胞かといった「運命決定」の分子メカニズムはほとんど知られていませんでした。
そこで今回、神経幹細胞の運命決定を制御する分子、特にごく微量の発現で遺伝子を調整する機能を持つ転写因子を見つけることを試みました。転写因子はリン酸化によってシグナルのオン・オフを制御しています。しかし、もともと生体内での発現が少なく、細胞の核内にごく微量しか存在しないことから、その現象を捉えることが難しいという問題点がありました。
そこで、転写因子を含む重要な核内因子を同定するために、細胞増殖因子(FGF2)による刺激を与えた神経幹細胞から核タンパク質を抽出しました。FGF2は繊維芽細胞増殖因子と呼ばれ、幹細胞を未分化のまま維持したり増殖させたりするのに重要な刺激を与える因子です。抽出した核タンパク質はプロテオミクス(タンパク質解析技術)を用いて分離し、その中からリン酸化するタンパク質を特異的に染色して質量分析器で探索した結果、新たな核内リン酸化タンパク質「Matrin-3」を発見しました。
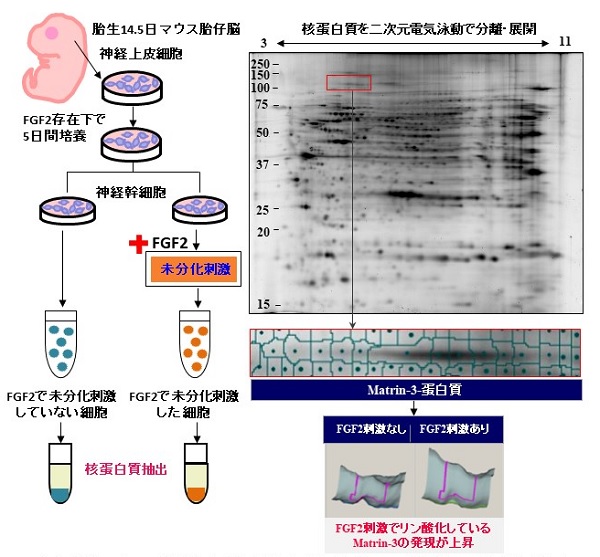
Matrin-3の発現とリン酸化は神経幹細胞の未分化性を維持する
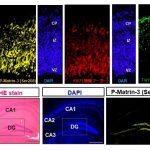
マウスの胎仔脳から採取・培養した神経幹細胞に、増殖因子(FGF2)を用いて未分化刺激を与えたところ、Matrin-3が高発現しリン酸化が進んでいることが明らかになりました。また、胎生期の脳におけるMatrin-3の発現を調べたところ、Matrin-3は神経幹細胞が豊富に存在する「脳室帯」「脳室下帯」「海馬歯状回」と呼ばれる領域に多く発現し、さらにそれらの領域においてMatrin-3はリン酸化していました。
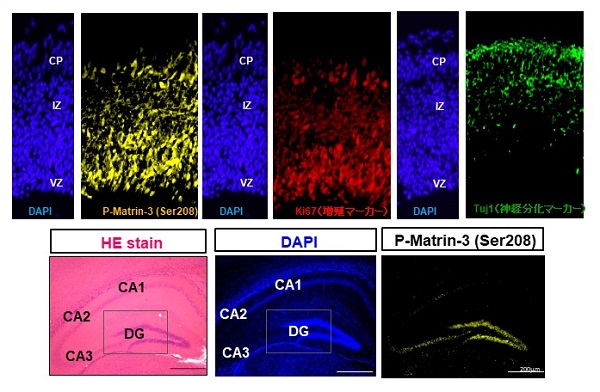
神経幹細胞が豊富な脳室帯、基底部、海馬歯状回においてリン酸化Matrin-3の亢進が認められた
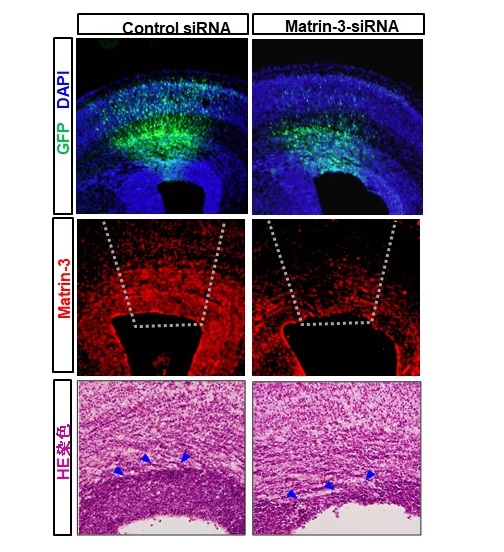
一方、Matrin-3を欠損させると、試験管内実験では神経幹細胞の突起伸長やニューロンへの分化を引き起こし、マウスを用いた生体実験では胎生期の脳層構造(大脳皮質に特有の層状の構造)の一部を破綻させました。このことから、Matrin-3が脳の発生において神経幹細胞の未分化性維持に重要であることがわかりました。
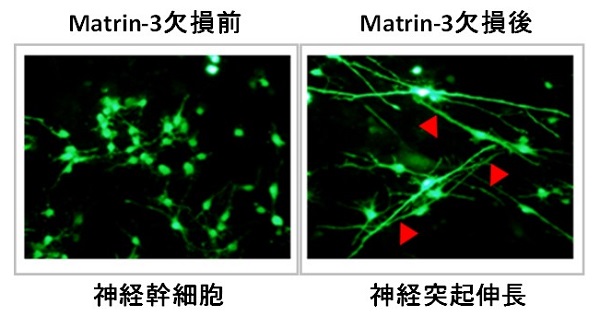
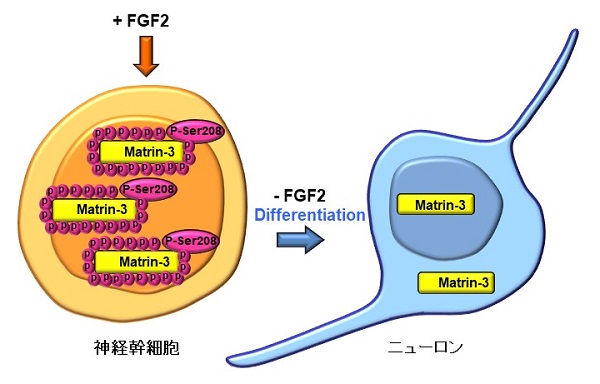
さらに、Matrin-3のリン酸化の機能を解明する実験を行った結果、Matrin-3のアミノ酸配列のなかでも特定の場所(208番目のセリン残基)が特定の酵素(ATMキナーゼ)によってリン酸化されることが、神経幹細胞の未分化性維持に重要であることがわかりました。
今回、筆者独自の技術を応用したプロテオミクス研究によって、神経幹細胞の運命決定を司る核内リン酸化タンパク質Matrin-3を発見し、Matrin-3の発現とリン酸化が、増殖因子FGF2による神経幹細胞の未分化性を維持する運命決定に必要であることを実証しました。
Matrin-3と家族性ALS – 近年の報告より
近年の研究報告から、Matrin-3の遺伝子変異が家族性筋萎縮性側索硬化症(家族性ALS)を引き起こす責任遺伝子であることが判明しました。 Matrin-3の遺伝子変異によって生じる神経分化を制御する因子の機能不全や、シグナル伝達をオン・オフする機能の崩壊(混乱)が、正常なシグナル伝達と脳発生を損ない神経系の障害をもたらしていることが考えられます。今回の研究成果は、家族性ALSの疾患メカニズムを解明するうえでも重要な手がかりになる可能性があります。
タンパク質の可能性 – 疾患マーカーや創薬の開発へ向けて
今回は、Matrin-3というタンパク質に関する研究についてご紹介しましたが、みなさんはタンパク質(プロテイン)の語源をご存知でしょうか? それは古代ギリシャ語の「プロテイオス」に由来し、「一番大切なもの」を意味します。私たちのからだを司っている重要な構成成分である「タンパク質」の機能を解明することは、生命の根幹を解明することに繋がります。
生体内の細胞や組織における「タンパク質」の構造・機能を総合的に研究することをプロテオミクスと呼び、プロテオーム解析はタンパク質の分離や同定技術のことを指します。今回の研究では、プロテオミクス解析の手法のひとつである二次元電気泳動法を応用させた独自の技術を確立しMatrin-3を発見しました。二次元電気泳動法は、タンパク質試料をゲル上でX軸とY軸方向に展開する方法で、タンパク質のもつ等電点と分子量により分離します。この方法は、タンパク質翻訳後修飾のひとつである「リン酸化」も捉えることができます。
たとえば、病気の原因を解明したいとき、二次元電気泳動法は分離能が優れているので、正常組織の試料と疾患組織の試料をそれぞれ二次元電気泳動により分離し、サンプル間でのタンパク質プロファイルを比較解析することが可能になります。そうすると、疾患特異的に増減を示すタンパク質を発見できます。もし癌特異的に発現するタンパク質があれば、それは腫瘍マーカーになる可能性があり、癌特異的に発現するタンパク質を抑制するような物質・方法を見つけることができれば、癌治療法や抗癌剤の開発に繋がります。今、癌の悪性度を司る原因タンパク質を見つけ、それを利用した抗癌剤をつくることを目指して一生懸命研究を進めているところです。
参考文献
Kanako Niimori-Kita et al., Matrin-3 is essential for fibroblast growth factor 2-dependent maintenance of neural stem cells, Scientific Reports, 8, 13412 (2018) doi:10.1038/s41598-018-31597-x
この記事を書いた人

-
熊本大学 大学院生命科学研究部(基礎系)分子病理学分野 助教。大阪大学大学院 理学研究科 生物科学専攻・蛋白質研究所(博士後期課程)修了 博士(理学)。2015年・2014年 熊本大学研究活動表彰 連続受賞。
今回の神経幹細胞やプロテオミクスの研究だけでなく悪性度の高い癌に対する治療法の開発などさまざまな研究を展開しています。2016年、熊本大学では研究者が有する技術で熊本地震から復興することを目的とした「熊本大学復興支援プロジェクト」が立ち上がり、私はその中の「産業復興プロジェクト」を拝命しています。ここでは私の有する独自の技術を用いて地場産業の新商品を生み出すべく地元企業と共同研究開発を行っています。「タンパク質をカギに人々の助けになる研究」を心掛けています。