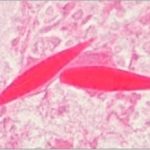
細胞の自爆で体内に結晶ができる? – アレルギーでみられる「シャルコー・ライデン結晶」のできる仕組みを解明!
シャルコー・ライデン結晶とは?
19世紀、日本では黒船来航で大騒ぎになっていた頃のことです。顕微鏡を使って解剖病理学を研究していたフランスのシャルコー教授は、病気の患者さんの体から、細長いひし形の小さな結晶を発見しました。その後ドイツのライデン教授も、喘息の患者さんの痰の中に同様の結晶を確認しました。
これは現在、シャルコー・ライデン結晶と呼ばれており、痰だけでなく、鼻水、便、尿、胸水(胸腔に溜まる液)、そのほか体のさまざまな部位で見つかることがあります。健康な人にできることはなく、喘息などのアレルギー疾患、寄生虫感染などに伴って現れることから、医師のあいだでは、シャルコー・ライデン結晶はこのような病気の特徴として知られてきました。体内で結晶ができるのは人体にとって異常なことのはずです。しかし、いったいどのようにこの結晶ができるのでしょうか?
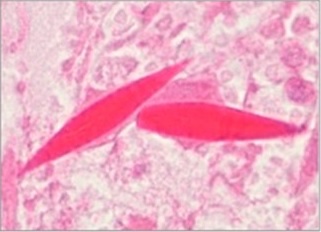
好酸球とシャルコー・ライデン結晶
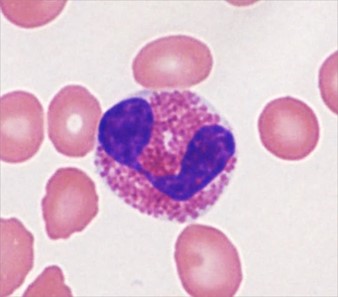
おもしろいことにシャルコー・ライデン結晶は、好酸球という白血球の一種が集まっているところに一致して出現します。好酸球は、ふつう血液中で白血球の1~4%くらいを占める数の少ない細胞ですが、アレルギーや寄生虫感染などで増加し、炎症が起こっている部分にアメーバ様の運動によって移動します。
たとえば肺に寄生虫が入り込んでいると、好酸球はその周りにびっしりと集まり、寄生虫の攻撃をしたり、その周りを固く変化させたりするのに役立っています。一方で喘息であれば気管支に、アレルギー性鼻炎であれば鼻の粘膜に集まって炎症を起こします。本来このようなアレルギーは体にとって不要な反応ですので、好酸球は役に立つこともあれば、むしろ悪者として働いてしまうこともあります。
私たちは医師としてさまざまな病気の患者さんの診断や治療を行いながら、特にこの好酸球という細胞に注目して研究しています。好酸球がどんなことをしているのかわかれば、好酸球の関係する病気を診断したり治療したりするのに役に立つからです。
好酸球の自爆と結晶
アレルギーが起こっている部位を電子顕微鏡などで詳しく調べると、好酸球が集まっているだけでなく、集まった好酸球が原因不明の細胞死を起こしていることが知られていました。2010年頃、筆者はアメリカで研究していたのですが、この現象をはっきりさせるため、毎日のように好酸球の「死」を調べていました。
いろいろな実験の結果、好酸球はある条件になるとエトーシス(ETosis)と呼ばれる特別な細胞死を選択することがわかりました。つまり、どうやら炎症のひどいところでは、好酸球は長生きをして働くというよりも、自らを「自爆」させて、中に入っている炎症物質をばらまいていたのです。言い換えれば、本来エトーシスは好酸球が体内に入ってきた病原体と戦うための最後の手段だったのです。異国の地で朝から晩まで好酸球を調べてこの細胞にすっかり感情移入してしまっていた筆者は、その壮絶な一生に「大和魂」を見いだした気がしました。好酸球から、「自分は何のために死ぬべきか」を考えさせられてしまうことになるとは思いもよりませんでした。
いつものように好酸球の細胞死を調べる実験をしていたある日のことです。顕微鏡で一定時間ごとに好酸球を撮影して動画を作成していると、エトーシスで細胞が壊れる直前、細胞の中に「ニョキ」という感じで、細長いひし形の物体ができるのを偶然見つけました。時間にすると1分足らずのあいだに、それまで何もなかった細胞の中にできた物体です。初めは何なのか理解するのに時間がかかりましたが、文献を確認してみても、シャルコー・ライデン結晶としか言い様のない形状でした。それまでまったく気にとめなかったのですが、一度見つけるとちょくちょく細胞の中に結晶ができていることに気付きます。死にゆく細胞の中に突如として現れる結晶……いったい何が起こっているのか興味がわきました。
シャルコー・ライデン結晶とアレルギー疾患
2012年、筆者が日本に帰国してから、耳鼻科や呼吸器科の医師、電子顕微鏡や病理学の専門家の協力を得て研究をすすめることができました。私たちは好酸球が増える難治性のアレルギー(好酸球性副鼻腔炎など)をもつ患者さんたちから採取された組織を、電子顕微鏡や蛍光顕微鏡で観察したり、病気の重症度別に光学顕微鏡で観察しシャルコー・ライデン結晶の数を調べたりしました。この結果、シャルコー・ライデン結晶は病気の重症度が上がるほどできやすいこと、また、出現する場所には好酸球が数多く集まるだけでなく、常にエトーシスを起こしていることがわかってきました。
シャルコー・ライデン結晶ができるメカニズム
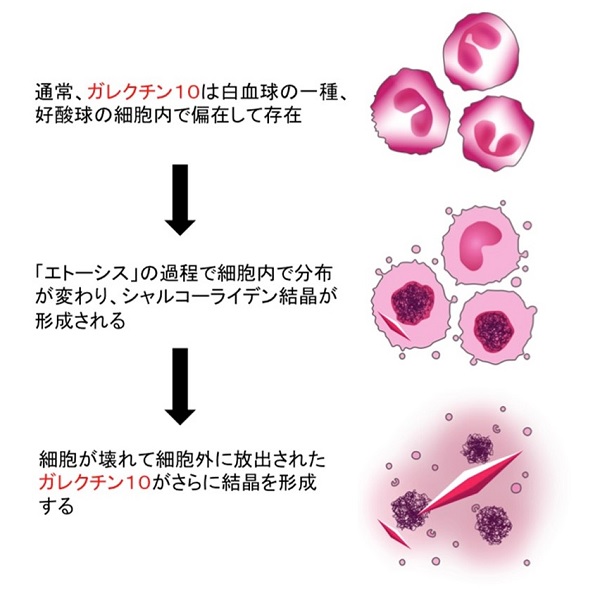
シャルコー・ライデン結晶の元になる蛋白であるガレクチン10(シャルコー・ライデン結晶蛋白ともいわれる)は、好酸球に多量に含まれています。私たちは採血した血液から分離した好酸球にエトーシスを誘導する物質を加えて培養し、細胞内でのガレクチン10の分布を観察しました。
これまでガレクチン10は顆粒(好酸球の中にある赤い粒)の中にあるとわいれていましたが、顆粒ではなく、ガレクチン10は好酸球の細胞質の端に偏在していました。好酸球が活性化してエトーシスを起こす過程で、ガレクチン10は細胞内に均一に分布するようになり、細胞内の位置が大きく変わっていく様子が観察され、細胞の中で結晶化する瞬間も初めて捉えることに成功しました。
最終的にエトーシスでは細胞が壊れますが、そうすると細胞内のガレクチン10が放出され、細胞外で濃度が上がります。このため、たくさんの好酸球が集まった状態であれば、細胞外のガレクチン10によって結晶が作られることもわかりました。さらに、エトーシスの過程を人為的に阻害する試薬を用いると、シャルコー・ライデン結晶の形成も抑制されることが確認されました。これらのことから、好酸球のエトーシスによってシャルコー・ライデン結晶が形成され、両者は密接に関係していることがわかりました。
今後の展開
発見から150年以上が経っているにも関わらず、シャルコー・ライデン結晶の出現機構の詳しい仕組みはよくわかっていませんでした。今回の研究により、この謎は分子・細胞学的な観点から明らかになりました。好酸球が特殊な細胞死を起こす過程で、ガレクチン10を制御しなくなることが結晶化の原因といえます。
ほかに体の中に結晶ができる例としては、痛風があります。痛風では体の中に増えた尿酸が結晶化して、関節痛などを起こします。最新の研究によると、シャルコー・ライデン結晶の存在自体が炎症を悪化させる原因になっているようです。このようにシャルコー・ライデン結晶の生成は、好酸球がアレルギー疾患の炎症を悪化させるメカニズムのひとつということができます。
ガレクチン10は体内ではほとんど好酸球だけにしか存在しません。臨床の場においては、シャルコー・ライデン結晶ができることや、ガレクチン10の濃度上昇は、エトーシスという特殊な好酸球の細胞死を間接的に示す指標となると考えられます。病気の診断や治療選択に役立つ可能性はどうか? エトーシスを防ぐことで治療に役立つか? など、今後も検討の課題は多くあります。この不思議な細胞 – 好酸球から、まだまだ病気を探っていく必要がありそうです。
参考文献
この記事を書いた人

-
植木重治
秋田大学大学院総合診療・検査診断学講座 准教授(医学博士)。呼吸器専門医・アレルギー専門医・臨床検査医学専門医。アレルギーの治療につながる炎症メカニズム、感染制御のネットワーク形成、検査医学に特に興味をもっています。好酸球に関する最近の研究はこちらもご参照下さい。http://www.med.akita-u.ac.jp/~gimclm/research.html
福地峰世
秋田大学大学院総合診療・検査診断学講座 大学院生・歯科医師。アレルギーにおける好酸球性炎症を研究しています。
イラストは好酸球くん(オリジナルキャラクター)