量子化学計算を駆使したキラル触媒設計で未達成不斉ホウ素化反応を実現!
有機ホウ素化合物とは?
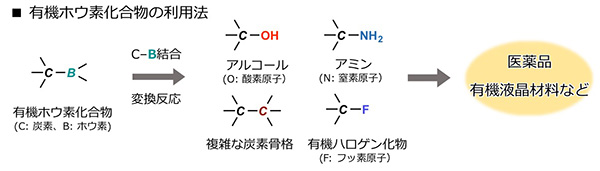
有機ホウ素化合物は、その炭素-ホウ素結合をさまざまな原子との結合へと変換することができる“ブロック”のように利用することができます。そのため、医薬品合成や液晶材料合成に広く用いられています。そのなかでも、現在世界中で多く利用されている有機反応のひとつである鈴木-宮浦クロスカップリングは、有機ホウ素化合物の特性を応用した革新的分子変換反応です。この反応を開発した北海道大学 鈴木章名誉教授は2010年にノーベル化学賞を受賞しています。ホウ素という元素は有機化合物を効率的に合成するうえで非常に重要な元素のひとつであるといえます。
銅触媒によるホウ素化反応を用いて未達成反応に挑戦
有機ホウ素化合物を用いた変換反応は近年、著しい発達を遂げており、特にキラルな炭素-ホウ素結合を有する、光学活性有機ホウ素化合物の重要性は医薬品合成の分野において高まってきています。当研究室では銅触媒を用いた光学活性有機ホウ素化合物の合成法の開発を行っています。
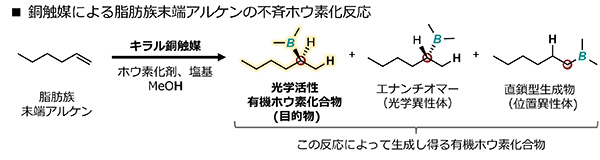
私たちは、非常に安価で手に入れることが可能な脂肪族末端アルケンに対して、銅触媒を用いた不斉ホウ素化を検討しました。これまでに報告されているホウ素化反応を用いた脂肪族末端アルケンへのホウ素化では、光学活性ではない(アキラル)な直鎖型のホウ素化を与えるものしかありませんでした。そのため、この反応を開発することができれば、有機合成化学に大きなインパクトを与えることができると期待されました。
そこで、まず、反応に使用する銅触媒を不斉反応用に「キラル銅触媒」にする必要があります。しかし、キラル触媒による脂肪族末端アルケンの位置選択的な不斉反応の開発例は非常に少なく、困難な課題でした。ところで、量子化学計算の分野は著しい発展を遂げている最中であり、その計算精度は非常に高いものとなっています。そこで私たちは、量子化学計算によって反応を詳しく解析することで、より効率的にこの反応に最適なキラル銅触媒の開発を行うことができると考えました。
不斉配位子の開発
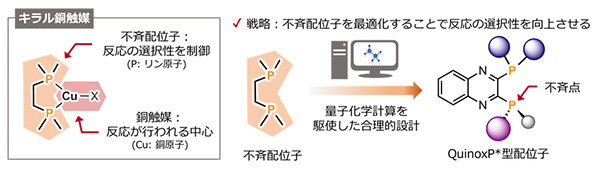
キラル金属触媒による不斉反応は、その金属に結合して働く「不斉配位子」によって反応の選択性を制御することが可能です。しかし、有機合成化学における不斉反応の開発というものはしばしば非常に困難です。これはそのエナンチオ選択性を発現させるメカニズムが明確でないなかで、膨大な量の実験を繰り返しながら、手探りで最適な不斉配位子や反応条件を探していく必要があるためです。研究をスタートするにあたり、何よりもその反応と相性が良い配位子を探すことが重要です。
私たちがまず着目したのが、2012年に日本化学工業株式会社の今本恒雄技術顧問(千葉大学名誉教授)らによって報告された、「QuinoxP*型配位子」です。QuinoxP*型配位子は2つのホスフィン部位と剛直な分子骨格を有する配位子であり、さらに、他の不斉配位子にはあまり見られない、ホスフィン部位のリン原子上に不斉点を有するという特徴を持っています。この不斉配位子を用いて実際に反応を行ったところ、中程度エナンチオ選択性で目的の光学活性有機ホウ素化合物が、主生成物として得られてきました。
量子化学計算を用いた不斉配位子のデザイン
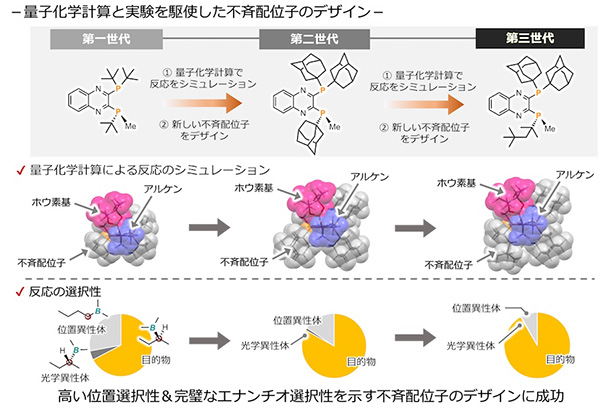
続いて、この実験結果に基づいた量子化学計算を行いました。この時、分散力という原子同士の弱い吸引的な力(ファンデルワールス力)を含む計算方法を選択することが成功の鍵でした。その結果として、実験結果である目的の光学活性有機ホウ素化合物を与える選択性を、非常に高い精度で再現することに成功しました。
この計算結果から、反応の選択性に影響が生じる箇所を探し出し、次世代の不斉配位子の設計指針として、新たな不斉配位子を合成しました。このように、実際の実験と量子化学計算を組み合わせた解析法を駆使することで、新配位子の開発世代を重ね、第三世代まで不斉配位子を最適化するとほぼ完璧なエナンチオ選択性(99.5:0.5)で、目的の光学活性有機ホウ素化合物を得ることに成功しました。
このようにして開発された不斉配位子を用いた脂肪族末端アルケンの不斉ホウ素化反応は、さまざまな脂肪族末端アルケン基質に対して非常に幅広い基質一般性を示しました。特に、工業原料のモデル化合物として、蒸留により分離が困難な炭素-炭素二重結合の位置が異なる異性体が混在している粗生成物をこの反応に用いた実験も行いました。その結果、このような原料を用いた反応であっても、完璧な選択性で炭素鎖の末端に二重結合を有するもののみが反応し、非常に高い選択性で目的の光学活性有機ホウ素化合物を与えることに成功しました。
量子化学計算と実験化学のコラボレーション
近年、量子化学計算は急速な発展を遂げています。実験化学者が得られた結果をもとに、理論化学者が量子化学計算を用いて反応機構を解明する試みは非常に多く報告されています。またこれまで研究者らによって想像もされていなかった、新たな反応機構を見つけることもあります。
一方で、理論化学と実験化学のあいだには未だに多くの壁が存在するように感じます。実際に目で見ることができない化学反応を、量子化学計算によってシミュレーションできるようになるということは、実験化学者にとっても反応開発を行ううえで非常に魅力的なツールであると言えます。
私たちのこの研究は有機合成化学において、実験により得られた結果を、量子化学計算を用いて解析し、新たな触媒を設計し、それを再び実験により検証し、量子化学計算で評価するという、実験と理論を組み合わせた反復型開発の成功例であると考えています。さらに、これからの有機合成化学において、未だ達成されていない、または、想像もされていない反応を、これらを上手に組み合わせて相乗効果で効率的に開発することができれば、新たな医薬品の開発や低価格化に大きく貢献できると期待されます。
参考文献
この記事を書いた人

-
岩本紘明(写真右)
北海道大学大学院総合化学院博士後期課程3年
2014年北海道大学工学部 応用化学コース卒業。2016年同大学大学院総合化学院において修士課程修了。2016年同大学大学院総合化学院において博士課程に進学。2016年から日本学術振興会特別研究員(DC1)。
今本恒雄(写真中央)
日本化学工業株式会社 研究開発本部技術顧問・千葉大学名誉教授
1972年大阪大学大学院理学研究科有機化学専攻博士課程修了 理学博士。1972年日本学術振興会奨励研究員。1973年大阪大学産業科学研究所助手。1975 年ミシガン州立ウェイン大学博士研究員。1978年東京大学理学部研究生。1980年千葉大学理学部助手。1988年千葉大学理学部助教授。1993年千葉大学理学部教授。2007年千葉大学大学院理学研究科教授。2008年千葉大学名誉教授。
伊藤肇(写真左)
北海道大学大学院工学研究院 教授
1996年京都大学大学院工学研究科博士課程修了 工学博士。1996年筑波大学化学系 助手。1999 年岡崎国立共同研究機構分子科学研究所 助手。2001年米国スクリプス研究所 客員研究員。2002年北海道大学大学院理学研究科化学専攻 助教授。2010年北海道大学大学院工学研究院 教授
この投稿者の最近の記事
 研究成果2018年8月22日量子化学計算を駆使したキラル触媒設計で未達成不斉ホウ素化反応を実現!
研究成果2018年8月22日量子化学計算を駆使したキラル触媒設計で未達成不斉ホウ素化反応を実現!



