生物の多様な形状の起源とは? – 集合体の形は分子認識相互作用の強さで決まる
分子認識によって形成される集合体の形はどのように決まるか?
生物のさまざまな形は、細胞同士がその表面に存在する分子の分子認識を介して、特定の位置や配列で集合(自己組織化)することにより形成されます。生体は、この分子認識に基づいた自己組織化によって形成される巨視的集合体です。生体系の巨視的集合体に触発され、多くの研究グループが分子認識を基盤とするスマート材料を開発しています。
以前、私たちは分子認識部位として環状オリゴ糖であるシクロデキストリン (CD) 残基と、CDの空洞に取り込まれるゲスト部位を導入したミリメートルスケールのポリアクリルアミドヒドロゲルを用いることによって、分子認識を肉眼で観察することに世界で初めて成功しました。その研究の過程で、分子認識部位の相互作用が強い場合にはゲルは交互の線状集合体を形成するのに対し、分子認識部位の相互作用が弱い場合にはチェック模様の面状集合体が形成する傾向を示すことに気づきました。
そこで私たちは集合体の形状と相互作用の強さの相関関係を調べるために、化学的に修飾することが容易で入手しやすい粒径200 μm程度の高吸水性ポリマー (SAP) の球状マイクロ粒子に着目しました。この記事では、SAPマイクロ粒子にβ-シクロデキストリン (βCD) 残基とアダマンタン (Ad) 残基を導入し、そのSAPマイクロ粒子の相互作用と得られた集合体の形状を調査した研究について紹介します。
分子認識に基づいたマイクロ粒子の集合体形成
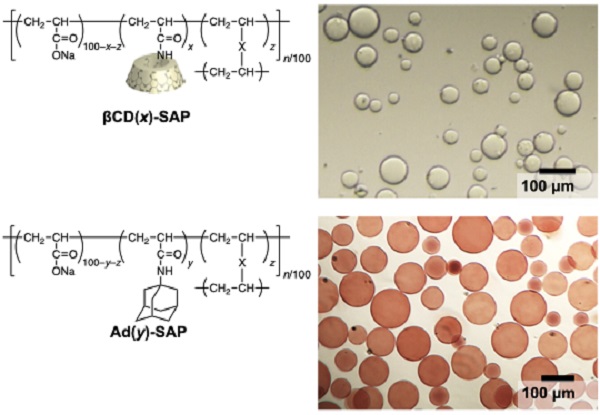
βCD残基とAd残基を導入したβCD(x)-SAPマイクロ粒子、Ad(y)-SAPマイクロ粒子を準備し、両者を識別するためにAd(y)-SAPマイクロ粒子をパラローズアニリンという赤色色素で染色しました。
ここで、xとyはβCD残基とAd残基のSAPマイクロ粒子への導入率を示します。x = 16.2, 22.3, 26.7 mol%の3種類のβCD(x)-SAPマイクロ粒子と、y = 5.2, 7.1, 10.7, 15.1 mol% の4種類のAd(y)-SAPマイクロ粒子を調製して用いました。
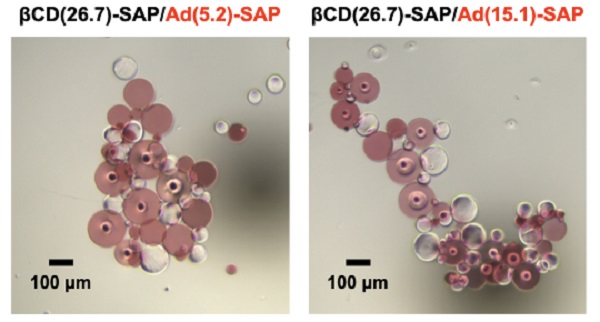
βCD(x)-SAPマイクロ粒子とAd(y)-SAPマイクロ粒子の相互作用を調査するため、それぞれの懸濁液を混合しました。今回使用したSAPマイクロ粒子は比較的大きく、ほとんどブラウン運動しないため、ピンセットを用いて混ぜたり、撹拌器で混合したりすることで集合体が形成されるかどうかを調査しました。
βCD(16.2)-SAPマイクロ粒子とβCD(22.3)-SAPマイクロ粒子は、今回用いた全てのAd(y)-SAPマイクロ粒子とは集合体を形成しませんでしたが、βCD(26.7)-SAPマイクロ粒子はすべてのAd(y)-SAPマイクロ粒子と集合体を形成しました。この結果は、集合体形成のためのβCD残基の導入量の閾値が22.3と26.7 mol%のあいだにあることを示しています。
マイクロ粒子の分子認識相互作用の強さ
以前の私たちのヒドロゲルによる巨視的集合体の研究では、引っ張り試験機で得られた集合体の破断強度を測定することが可能で、その結果から相互作用の強さを評価することができました。しかし、今回は引っ張り試験機を用いることができないためにSAPマイクロ粒子同士の相互作用の強さを比較することは困難でした。たとえば、集合体形成の所要時間を計測したり、集合体の形成過程の観察を試みたりしましたが、相互作用の強さを評価することはできませんでした。
最終的には、SAPマイクロ粒子同士の相互作用を阻害する競争分子、すなわちβCDとアダマンタンカルボン酸ナトリウムを添加した際に、集合体を構成するSAPマイクロ粒子の数を計測し、単純化したモデルを用いて解析することで、SAPマイクロ粒子同士の相互作用の強さを比較することができました。
予想通り、アダマンタン残基導入率yの高いAd(y)-SAPマイクロ粒子ほどβCD(26.7)-SAPマイクロ粒子と強く相互作用することがわかりました。
マイクロ粒子集合体の形状と分子認識相互作用の強さの関係
次に私たちは、βCD(26.7)-SAPマイクロ粒子とAd(y)-SAPマイクロ粒子が形成する集合体の形状を比較する方法を検討しました。
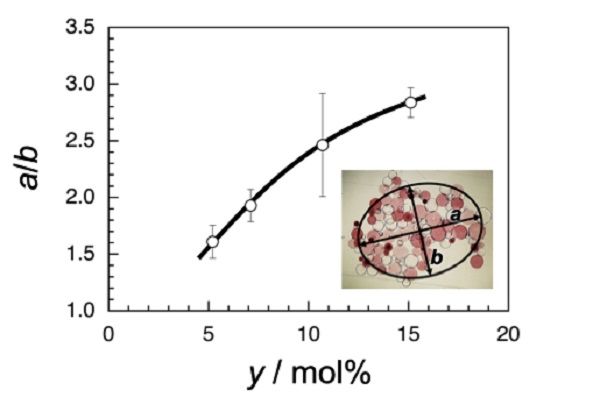
はじめに、ひとつのマイクロ粒子が接触するマイクロ粒子の数である配位数に着目しました。一次元に伸びた集合体の場合、配位数は2となり、平面状集合体ならば4や6となるはずです。しかし、粒子数が多く手間がかかるため、配位数の決定は現実的ではありませんでした。したがって、比較的良く利用されている画像の楕円近似により長軸 (a) と短軸 (b) の比、つまりアスペクト比 (a/b) を用いて集合体の形状を評価することにしました。
同じ実験を3回繰り返してa/bを決定し、その平均値をyに対してプロットすると、yが5.1 mol%から15.1 mol%まで増加するとともに、アスペクト比a/bは1.6から2.8まで増加する傾向を示しました。
先に述べたように、yの増加とともにSAPマイクロ粒子同士の相互作用が強くなるため、相互作用が強い場合には伸びた集合体を形成し、相互作用が弱い場合には平面的な集合体を形成することが明らかとなりました。
相互作用の強さによってマイクロ粒子集合体の形状が変化する理由
これらの結果は、以下のように定性的に説明できます。攪拌後初期に形成した少数のSAPマイクロ粒子からなる小さな集合体は、さらに衝突して大きな集合体へと成長していきます。その際、SAPマイクロ粒子の相互作用が強い場合は、1点で接触しても接着しますが、弱い相互作用の場合、複数の点で接触した場合にのみ集合体が成長すると考えられ、アスペクト比と相互作用の強さとの相関関係が説明できます。
ブラウン運動する小さなコロイド粒子の凝集については古くから研究が行われています。そこで今回のSAPマイクロ粒子の結果をコロイド凝集理論と比較することにしました。コロイド凝集が起こる際、コロイド粒子間の相互作用が強く、衝突すると必ず凝集が起こる拡散律速機構と、衝突した際になんらかの反応が起こらないと凝集しない反応律速機構が知られています。また、それぞれの機構で形成される凝集体は、フラクタル構造となることが知られています。
コロイド凝集体の質量と半径をそれぞれM、Rとすると、M ∝ RDfで表されるフラクタル次元Dfは、拡散律速機構では1.75、反応律速機構では2.05であることが知られています。
Tunable Limited Aggregationソフトウェアを用いてコロイド粒子数N = 15, 30, 100, 200に対してDf = 1.75, 2.05となるように構築した凝集体を比較すると、拡散律速機構 (Df = 1.75) の方が疎で広がった凝集体となることを示しています。
特に小さなN (= 15) の凝集体に着目し、二次元平面への投影図に対して楕円近似を行うとアスペクト比はそれぞれa/b = 1.75, 1.45と評価することができました。すなわち、本研究で得られた相互作用の強さとアスペクト比の関係は、粒子数の小さな条件におけるコロイド凝集理論で説明できることがわかりました。

生物が作る多様な形状との関係
このように相互作用の強さ、つまり分子認識部位であるAd残基の導入率yを変化させることで、集合体の形状を制御できることがわかりました。生物の形状の多様性がどのようにできたかは、まだまだ研究が必要です。しかし、生物が作る形状の多様性は、生物ができつつある過程で、相互作用の強さによって異なる形状の集合体が形成したことに端を発しているのかもしれません。
参考文献
・Macroscopic self-assembly through molecular recognition
Harada, A.; Kobayashi, R.; Takashima, Y.; Hashidzume, A.; Yamaguchi, H. Nat. Chem. 2011, 3 (1), 34-37.
・The macroscopic shape of assemblies formed from microparticles based on host–guest interaction dependent on the guest content
Itami, T.; Hashidzume, A.; Kamon, Y.; Yamaguchi, H.; Harada, A. Sci. Rep. 2021, 11 (1), 6320.
・A Simplified Model for Multivalent Interaction Competing with a Low Molecular Weight Competitor
Hashidzume, A.; Itami, T.; Kamon, Y.; Harada, A. Chem. Lett. 2020, 49 (11), 1306-1308.
この記事を書いた人
-
橋爪 章仁
大阪大学大学院理学研究科 教授
1997年3月大阪大学大学院理学研究科高分子科学専攻博士後期課程修了後、大阪大学大学院理学研究科高分子科学専攻助手、助教、講師、准教授を経て、2015年10月より現職。この間、客員研究員として、インディアナ大学・パーデュー大学インディアナポリス校化学科、イリノイ大学アーバナ・シャンペーン校化学科、カリフォルニア大学サンタバーバラ校材料科学研究所に滞在。2008年シクロデキストリン学会奨励賞、2013年高分子学会Wiley賞を受賞。
原田 明
大阪大学産業科学研究所 特任教授
1977年3月大阪大学大学院理学研究科高分子学専攻博士後期課程終了後、大阪大学理学部教務職員、IBM (San Jose) 研究所客員研究員、コロラド州立大学客員研究員、大阪大学産業科学研究所助手、大阪大学理学部高分子学科助手、助教授を経て、1998年4月大阪大学大学院理学研究科高分子科学専攻教授。2015年3月大阪大学定年退職後、4月より大阪大学大学院理学研究科特任教授、2019年4月より現職。IBM科学賞、大阪科学賞、高分子学会賞、シクロデキストリン学会賞、紫綬褒章、Izatt-Christensen International Award、日本化学会賞、高分子科学功績賞など多数受賞。




