典型元素触媒と水素を活用したクリーンなアミン変換法を実現!
アミンの還元的アルキル化反応、その理想的な形式を目指して
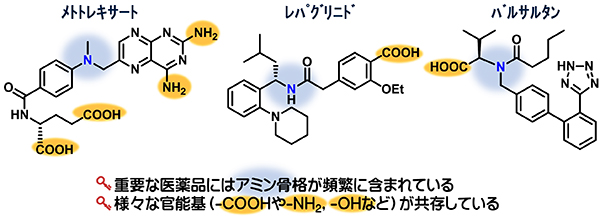
アミン(NR3、Nは窒素でRは炭素や水素など)は多くの医薬品、農薬、機能性材料、食品添加物などに含まれる重要な化合物です。たとえば、下図に紹介するメトトレキサート(抗癌剤、抗リウマチ薬)やレパグリニド(糖尿病薬)、バルサルタン(高血圧症治療薬)などもアミン(または、そこから誘導される)骨格を含んでいる化合物です。注目すべきことに、このようなアミンには複数のアミノ基(-NR2)が含まれていたり、カルボキシル基(-COOH)などの重要な官能基が共存しています。
アミン骨格を構築する信頼性の高い手法が、単純なアミン類の触媒的還元的アルキル化反応です。これは、反応の進行を助ける触媒が存在する条件下において、原料となるアミン、化学修飾を施すパーツとなるカルボニル化合物、そして還元剤から、より複雑なアミンを一挙に構築する手法です。
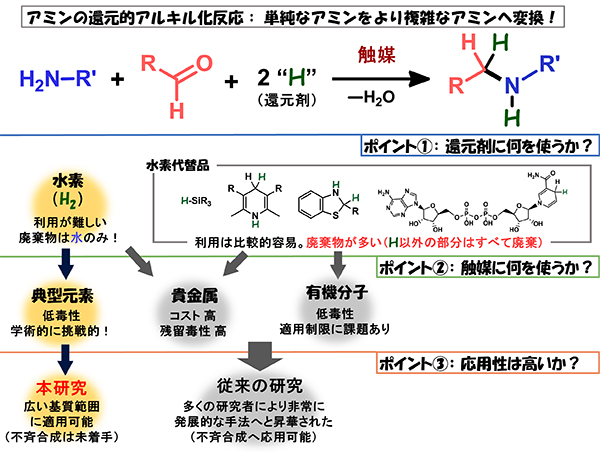
とくに、最近は『毒性の低い触媒を用いること』や『化学反応において発生する廃棄物を最小限に抑えること』の重要性が盛んに提起されており、医薬品などに頻繁に含まれるアミンだからこそ、なおさら、このような課題を解決した合成手法が求められています。
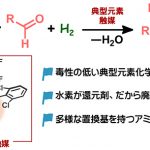
可能な限り廃棄物を減らす、という観点から考えると、水素(H2)を還元剤として利用するアミンの還元的アルキル化手法は、副生成物として水(H2O)のみを与えるため、環境調和性が高くクリーンであると言えます。しかし、従来の手法はH2を還元剤として用いるために、反応性の高い貴金属触媒を利用することが主流でありました。しかし、貴金属の利用には多くの問題が付随します(たとえば、貴金属の高い毒性やコスト、高額な残留金属の除去コスト、など)。
毒性の低い典型元素化学種を触媒として活用し、その上でH2を還元剤とするアミンの還元的アルキル化反応系が開発できれば、従来法の問題を解決した理想的なアミン合成法が実現できると期待できます。……しかし、どうすれば、高反応性な金属に頼ること無くH2を活性化し、アミンの還元的アルキル化に利用することができるのか? これは、長年解決が待ち望まれてきた有機化学の課題でした。
鍵は有機ホウ素化合物の利用! 理想の実現への一歩
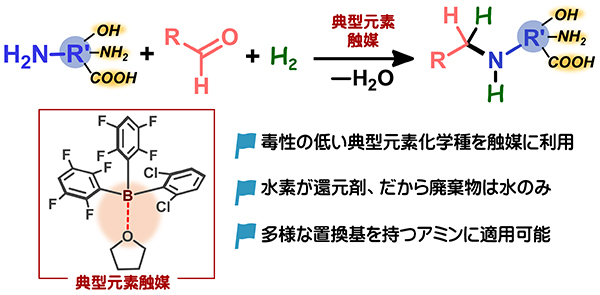
今回、私たちの研究グループは、ハンガリーの研究者らが開発した有機ホウ素化合物とテトラヒドロフランを組み合わせることで、H2を還元剤とするアミンの還元的アルキル化反応に適用可能な高活性触媒が発生することを発見しました。我々の手法の特筆すべき点は、従来法では適用が困難であったカルボキシル基(COOH)やヒドロキシル基(OH)を始め、非常に多様な官能基を備えたアミンをダイレクトに変換することができる応用範囲の広さです。
カルボキシル基を持つアミンはアミノ酸として知られており、たとえば、下の4-アミノサリチル酸は抗生物質として利用されています。これを我々の開発した反応の原料としてダイレクトに用いることで、4-アミノサリチル酸由来の重要な骨格を活かした新たなアミンを簡単に合成することが可能です(下図a)。さらに、分子内に複数のアミン部位を有する基質を用いた際、それらのアミンの微妙な環境の違いを敏感に見分け、片方のアミン部位のみを選択的に変換し、アミノ酸を一挙に合成出来ました(下図b)。残念ながら、天然アミノ酸の一種であるバリンそのものは溶解度の関係から用いることが難しかったのですが、その誘導体を効率的に変換することに成功しました(下図c)。
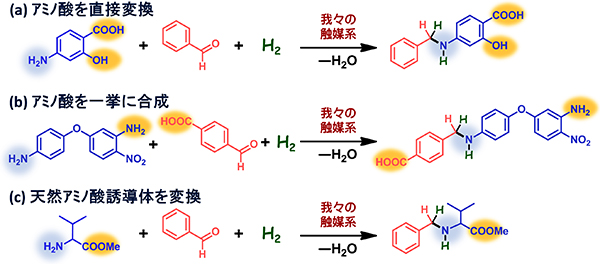
そして何よりも、我々の手法を利用した際の反応副生成物は水のみであり、同時に、毒性の高い元素を含まないため、非常にクリーンなアミン変換手法であると言えます。
まだまだ課題は尽きない、だから次の挑戦へ!
今回、我々は、触媒に有機ホウ素化合物、還元剤にH2を用いたアミンの還元的アルキル化反応を開発しました。我々の手法を用いることで、生理活性を備えたアミノ酸など多様なアミンをダイレクトに変換することが可能となりました。さらに、反応の副生成物は水のみです。また、毒性の高い貴金属類を一切用いていない点も、我々の手法の特筆すべき結果であると言えます。
しかし、まだまだ改善すべき点が残っていることも事実です。たとえば、反応の条件をより穏やかにする(反応温度を下げる、H2の圧力を下げる)ことで、エネルギーの無駄を減らすことができます。また、有機ホウ素触媒のパフォーマンスを向上させることで、コスト面での利点をより際立たせることができます。反応生成物の三次元的な立体制御にも挑戦しなくてはいけません。
これらは、我々が取り組むべき次の課題であり、より理想的かつ究極的なアミン変換法の開発を目指して、研究を続けていきたいと思っています。
本研究は大阪大学大学院工学研究科の生越專介教授が主催する研究室の成果です。研究チームのメンバーである木下 拓也君(博士後期課程)、ハズラ スニット博士(研究員)、大橋 理人准教授、生越教授らの代表として、私が本稿を寄稿させて戴きました。また、研究費は日本学術振興会から支援されました。
参考文献
- P. J. Dunn et al., Green Chem., 2007, 9, 411.
- T. Soós et al., ACS Catal., 2015, 5, 5366.
- Y. Hoshimoto et al., J. Am. Chem. Soc., 2018, 140, 7292.
この記事を書いた人

-
大阪大学大学院工学研究科応用化学専攻 講師
平成20年大阪大学工学部応用自然学科卒業後、同大学大学院工学研究科において博士後期課程に進学。平成25年に博士後期課程応用化学専攻を修了し、博士号(工学)を取得。この間、日本学術振興会特別研究員(DC1)。平成25年から平成30年の間、大阪大学大学院工学研究科 助教。平成30年より現職。専門は有機金属化学および有機典型元素化学。現在の研究課題は多機能・多用途カルベンの開発と応用、高反応性分子会合体と水素を活用した反応開発、低原子価遷移金属錯体の創成と応用。
受賞歴:第67回日本化学会 進歩賞、2014 IUPAC-SOLVAY Honorable Mention Award for Young Chemistsなど。
個人HP:http://www.chem.eng.osaka-u.ac.jp/~ogoshi-lab/hoshimoto/wp/
この投稿者の最近の記事
 研究成果2018年7月9日典型元素触媒と水素を活用したクリーンなアミン変換法を実現!
研究成果2018年7月9日典型元素触媒と水素を活用したクリーンなアミン変換法を実現!



