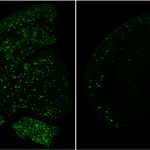
アミロイドβの蓄積を防ぐ遺伝情報の操作 – モデルマウスを使って保護的な遺伝子変異を探る
アルツハイマー病とは
認知症は超高齢社会である日本にとって身近な、そして極めて深刻な問題として存在しています。日本では400万人を超える認知症の患者さんが存在すると推計されており、みなさんも新聞やニュースで耳にする機会が多いと思います。認知症とは複数の疾患の総称なのですが、高齢期に発症する認知症の半数以上を占めているのがアルツハイマー病です。
アルツハイマー病は進行性の神経変性疾患であり、一度発症すると病状を完全に食い止めることはできません。徐々に記憶や認知機能が低下し、やがて自立した生活を送ることが困難になります。このため、患者さん本人の生活に深刻な影響が出るだけでなく、介護する身内の方にも大きな負担がのしかかります。
世界中で疾患克服のための研究が盛んに行われていますが、有効な治療法はまだ開発されていません。また、アルツハイマー病は20年、30年という長いスパンで発症に至ると考えられています。そのため、まだ発症していない段階で予防的な治療を行うのが良いとする流れもあります。しかし、発症していない健常者がその後の人生でどのくらいの確率で発症するのか、正確にリスク評価できる段階にもありません。
原因物質アミロイドβと発症につながる遺伝子変異
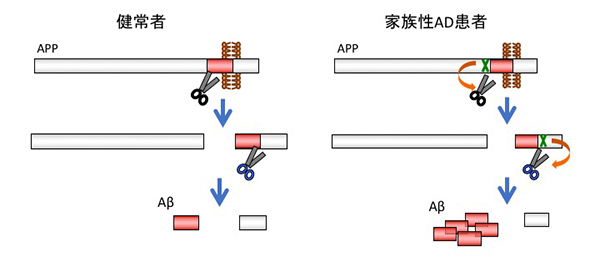
アルツハイマー病患者の脳には、約40個のアミノ酸からなるアミロイドβペプチド(Aβ)が凝集・蓄積し、老人斑と呼ばれる特徴的な病理像となります。Aβは1980年代半ばに初めて発見されました。その後、Aβと疾患発症との関係は家族性のアルツハイマー病患者を対象とした研究によって理解が進んできました。家族性の患者さんでは、Aβの前駆体タンパク質(APP)やAPPの切断に関わる遺伝子上に変異が認められます。そして、結果として生じるAβの産生増加や凝集性上昇が発症の引き金となります。
1990年前後からの家族性患者の家系に着目した遺伝学的な解析によって、発症原因となる遺伝子変異が300以上見つかっています。また、家族性だけでなく、大部分を占める孤発性の患者さんの発症にも遺伝的素因が少なからず影響することがわかってきています。近年の遺伝情報の解析スピードの劇的な向上により、アルツハイマー病患者と健常者の遺伝情報で何か違うのか、遺伝情報の網羅的な探索が行われるようになりました。数千人という規模の遺伝子情報を比較した結果、発症リスクを上昇させる遺伝子変異がこれまでに30以上同定されてきました。
一方、発症リスクを減少させるような遺伝子変異はまだほとんど見つかっておりません。発症リスクの上昇は疾患発症という目に見える結果として現れる一方で、発症リスクの低下は何も手がかりが出ないため、探索が難しいのです。
モデルマウス作製の過程で保護的変異のヒントが見つかった
私たちの研究グループは2014年、遺伝子ノックイン型のアルツハイマー病モデルマウスの作製に成功しました。従来型のモデルマウスは、外来遺伝子を過剰に発現するトランスジェニック型であり、ヒト患者脳と病態が異なっていたり、原因不明の突然死などの副作用が出たり、と問題がありました。この問題を改善するため、複数のアルツハイマー病の病的変異をマウスのAPP遺伝子領域に導入し、さらにマウスのAβのアミノ酸配列をヒトと同じ配列に変えました。その結果、ヒト患者脳と似たAβの蓄積が認められるようになったのです。
このノックイン型モデルマウス完成までの試行錯誤のなかで、意図したとおりに複数の遺伝子変異が導入されているにもかかわらず、脳内へのAβの蓄積がまったく認められない系統が見つかりました。この系統では、APP遺伝子の配列の一部が欠失していたため、欠失した遺伝子領域が何らかの役割を担っている可能性が考えられました。私たちは、本来の遺伝情報とは異なった数千の文字列のどこかにアルツハイマー病の原因物質Aβの蓄積に関係する領域があるはずと予想しました。
ゲノム編集技術を使った遺伝子領域の絞り込み
そこで、遺伝情報のどこの部分が大事なのか調べることにしました。今回は特に非翻訳領域に着目しました。非翻訳領域は遺伝子配列のなかでメッセンジャーRNAに転写されるものの、タンパク質には翻訳されない領域です。欠失の影響をマウス個体で直接調べるためにゲノム編集技術を使いました。ゲノム編集技術は狙った箇所を違う配列に変えることができる優れた技術ですが、今回は特定の遺伝子配列を切り取るという操作を行いました。モデルマウスの受精卵にゲノム編集ツールを打ち込んで、非翻訳領域のうち大部分に相当する700塩基を欠失させました。その後、モデルマウスの成長を待ち、通常ではAβが蓄積する時期に解析を行いました。
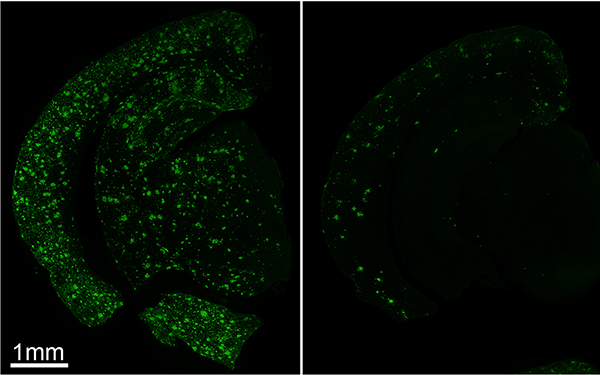
結果はクリアなもので、編集したモデルマウス脳内ではAβの蓄積が抑制されていました。次に、脳内Aβの定量的な評価を行なったところ、ゲノム編集の効率に依存してAβ産生量が下がることが確認できました。さらに、これらのマウスでは、APPのタンパクレベル(翻訳後の発現量)およびmRNAレベル(転写後の発現量)に応じてAβ蓄積量が変動していました。このことから、欠失させた遺伝子領域はAPPの発現量を調節していることが明らかになりました。欠失させる遺伝子領域を短くして、同様の実験を行ったところ、約400塩基を欠失させた場合でも、Aβ産生量の低下が認められました。最終的には、34塩基を欠失させただけで同様の現象が確認され、この34塩基がAβの蓄積の抑制に重要であることがわかりました。
さらなる保護的変異の同定を目指して
本研究では、モデルマウス作製の過程で偶然見つかった現象を出発点とし、ゲノム編集技術を駆使することでAβの蓄積に対して抑制的に働く遺伝的な欠失を発見しました。今回対象にした非翻訳領域はマウス・ヒト間で配列が似ているため、ヒトで実際の保護的変異の同定につながる可能性があります。
ヒト遺伝情報の大規模解析は極めてパワフルな方法ですが、あまりにも膨大なコストがかかるため誰にでもできる研究ではありません。また、コストを払ったからと言って確実に見つかるとも限りません。せっかく効果が高い変異が存在していても、その変異の頻度が低いと結果が埋もれてしまって上手くみつからないのです。大規模なヒト研究では人種も混在してしまいますが、人種間の遺伝情報の多様性も考慮すべき問題です。これまでに例外的にみつかっている効果の高い保護的変異は北欧の人たちでは200人に1人程度がもっていますが、それ以外のアメリカ、日本も含めてアジアの集団では桁違いに頻度が低いため、効果があるのかどうかはっきりしていません。
保護的変異は未発症者のリスク評価の改善、さらにはまったく新しい視点からの治療法の開発につながる可能性があります。いろんな分野の研究者が知恵を出し合って、効率的に同定していけると良いと考えます。
参考文献
この記事を書いた人

- 2010年 大阪市立大学医学研究科博士課程終了。日本学術振興会特別研究員(PD)、理化学研究所基礎科学特別研究員を経て、2017年より理化学研究所脳神経科学総合研究センター神経老化制御研究チーム研究員。遺伝子情報がどのように疾患に結びつくのかに興味をもって研究しています。特にアルツハイマー病、先天性関節拘縮症という2つの神経系の疾患に注目しています。家では3人の女性(妻、長女、次女)に振り回される日々。