水から水素をとりだす「半導体光触媒」の新たな設計指針 – 光励起電荷移動の制御で量子収率がほぼ100%に!
太陽光エネルギーで水から水素をとりだす
化石資源に依存しないエネルギー基盤の確保は、人類にとっての前世紀からの重要な課題です。クリーンなエネルギー利用手段として水素が注目されていますが、この水素は現在のところ化石資源から取り出されたものであり、資源の枯渇や二酸化炭素排出などの問題は回避できません。
この解決策として唯一考えられるのは、太陽光のエネルギーを用いて水を分解して水素を製造することです。この場合、エネルギーの起源は太陽光であり、水素は太陽エネルギーを使いやすいかたちで保存するためのエネルギーキャリアです。この水素を太陽光のエネルギーを使って水から取り出すためのさまざまな方法が検討されています。
そのなかでも我々は、「半導体光触媒」を用いた水の光分解について取り組んでいます。以下に、筆者らの最近の研究成果について紹介します。
半導体光触媒による水の光分解
光触媒を用いた水の光分解では、微粒子状の半導体粉末を水中に分散させ、光照射することで水素と酸素が生成します。半導体粒子がバンドギャップ以上のエネルギーをもつ光を吸収すると価電子帯の電子が伝導帯に励起され、価電子帯に正の電荷をもつ正孔と、伝導帯に負の電荷をもつ励起電子が生成します。
そして、それらの光励起電荷が半導体粒子の表面に移動し、正孔が水を酸化して酸素を生成します。そして、励起電子がプロトンを還元して水素を生成することにより水の分解反応が成立します。
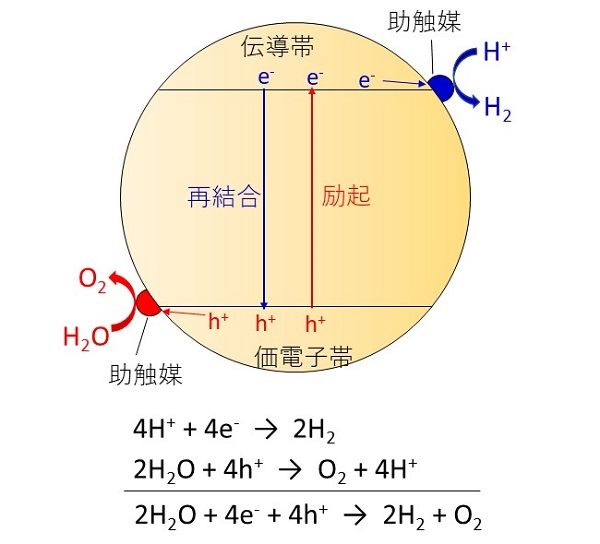
半導体光触媒を用いたこの手法は、原理的には太陽電池で水を電気分解するのと同じですが、粉末を水中に分散させて光を照射するだけで水素が得られ、簡易なシステムで稼働できるという観点からスケールアップに適していると期待されています。
高効率な光触媒をつくる鍵とは?
太陽光は地表に膨大な量のエネルギーを届けていますが、そのエネルギー密度が低いために広大な受光面積を確保できるシステムが不可欠となります。しかし、光触媒では1 μm(マイクロメートル)を下回るようなひとつの半導体微粒子の中で電圧を発生させ、なおかつ水素と酸素を形成する触媒機能まで組み込むことが必要となります。このため構造設計と制御が困難となり、効率も太陽電池に比べて低いことが問題となっていました。また、その構造設計の概念や方法も明らかになっていませんでした。
半導体光触媒を用いて水を水素と酸素に分解することが困難な理由は、この光化学反応が可逆的かつ多電子移動過程からなるためです。それらの多電子移動が完結して水素と酸素を取り出すまでのあいだに、逆方向の電子移動が競争して起こり得ます。むしろ、この逆電子移動のほうが熱力学的には優位になるため、差し引きすると目的の水分解反応の効率は非常に低くなりがちでした。
よって、この逆電子移動を抑え、順方向の電子移動のみを促進することが、高効率な光触媒を開発するための鍵となります。このような反応において、実際に100%に近い量子収率で水分解反応を進めることが可能かどうかはひとつの疑問でした。我々の最近の研究では、その問いに対して「可能である」という答えを実例とともに示し、それを可能とする触媒の構造と機能を明らかにしました。
「光励起電荷の異方的な移動」でほぼ100%の量子収率を達成
半導体光触媒による水の光分解では、ひとつの微粒子の中で励起電子と正孔が近い場所で同時に働くため、結果的にお互いに還元力も酸化力も弱め合うことになります。よって、ひとつの微粒子内で還元と酸化を上手く分けて行う必要があります。これを可能としたのが、光励起電荷の異方的な移動という効果です。
今回私たちが光触媒として用いたSrTiO3(Alドープ)は、ひとつの粒子がほぼ単結晶のドメインからなり、いくつかの異なる結晶面が露出しています。そして、ある特定の異なる結晶面に励起電子と正孔がそれぞれ選択的に移動する現象が知られていました。私たちは、この粒子表面に助触媒を担持して水素形成と酸素形成を促進しました。ここで助触媒は水の電気分解における電極触媒と同じ役割を果たします。
光電着法によって助触媒を担持すると、光励起電子が表面に移動して金属イオンを還元することにより金属を析出し、正孔が移動してきた表面では金属イオンを酸化して金属酸化物が析出し、それぞれが還元と酸化反応を促進する助触媒として機能します。この光電着法に異方的な電荷移動という性質が加わると、水素を形成する助触媒と酸素を形成する助触媒を異なる結晶面に選択的に析出させることができます。さらに、励起電子は水素生成助触媒、正孔は酸素生成助触媒へと選択的に移動するという都合の良いことだけが起こるという結果になります。
水素生成助触媒となるのがRhで、その表面を含水のCr2O3層で被覆することにより水素生成だけを促進し、逆反応となる酸素還元反応を完全にブロックします。そして酸素生成助触媒となるCoOOHも水の酸化反応のみを促進します。
従来の含浸法を用いた場合は助触媒粒子がランダムに半導体表面に分散しますが、その場合と比べて2倍程度水分解活性が向上し、量子収率は350~360 nmの範囲で100%に近い値となりました。つまり吸収した光のほぼすべてを水分解反応に利用できることがわかりました。量子収率の上限である100%に近い値で水分解を達成できたのは初めての例です。
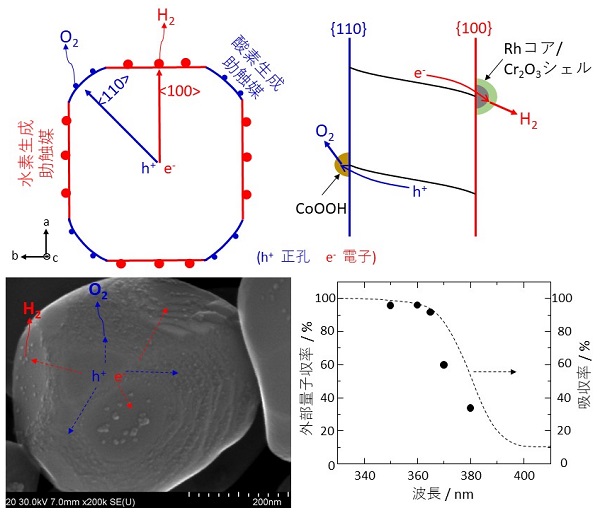
この光励起電荷が半導体粒子内で異方的に移動することの原因は、異なる結晶表面間で電位差があり、半導体粒子内で電位勾配が生じ、それに沿って一種の整流作用が働くからと考えられます。また、結晶表面間での電位差が生じる理由は、露出表面では少なからずイオンの解離・溶出があり、カチオンとアニオンのバランスが崩れて電荷が発生します。その度合いが結晶表面によって異なるために電位差が生じると考えています。ただし、この部分は現在のところ実測できていないため、今後解明していく必要があります。
今後の展望
光触媒による水分解において高い太陽エネルギー変換効率を達成するためには、太陽光スペクトルの中で幅広い波長範囲において高い量子収率で水分解反応を進める必要があります。この波長範囲は、用いる半導体の光吸収特性(バンドギャップ)で決まります。その波長範囲の理論上の限界が約1000 nmの波長になります。光触媒反応の素過程にある活性化エネルギーをより小さくしていくことによりこの限界値に近づけていくことが望まれます。
今回用いたSrTiO3は380 nmより短波長側の紫外光しか吸収しないため、よりバンドギャップの小さな化合物を利用していく必要があります。現実的な目標となる波長領域は、500 nm~600 nmより短波長側になります。その際にも、ここで紹介した触媒設計の指針は不可欠になると考えられます。
参考文献
Takata, T.; Jiang, J.; Sakata, Y.; Nakabayashi, M.; Shibata, N.; Nanadal, V.; Seki, K.; Hisatomi, T.; Domen, K.; “Photocatalytic water splitting with a quantum efficiency of almost unity” Nature, 2020, 581, 411-414.
この記事を書いた人
-
高田 剛(たかた つよし)
信州大学先鋭材料研究所 特任教授
[最終学歴] 2000年東京工業大学総合理工学研究科博士課程修了。博士(理学)。
[専門] 触媒化学
堂免 一成(どうめん かずなり)
信州大学 特別特任教授/東京大学 特別教授
[最終学歴] 1982年東京大学理学系大学院化学専門博士課程修了。理学博士。
[専門] 触媒化学、表面科学、材料科学




