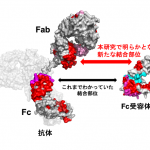
抗体に秘められた結合部位の発見 – 免疫分子の働く姿をリアルタイムで観測!
私たちを外敵から守る優れた免疫システムとは?
私たちの身体には、細菌やウイルスなどの外敵の侵入に対し、防御することで健康な状態を維持する免疫システムが備わっています。この免疫システムは、さまざまな免疫細胞や生体分子が関わり、協力し合うことで、侵入した外敵を速やかに排除するように働きます。
免疫システムが働くうえで特に重要な役割をするのが「抗体」です。抗体は私たちの体内に広く分布するタンパク質で、異物の侵入に応じて体内で随時作り出されます。抗体は異物を認識し捕まえた後に、他の免疫細胞などと協力することで、それらを無毒化または殺傷する役割を担っています。
しかしながら、抗体がどのように他の免疫細胞や生体分子と協力し、免疫機能が発動されるのか、詳細な分子メカニズムは明らかとなっていませんでした。
抗体が司る2つの免疫機能の発動モデル
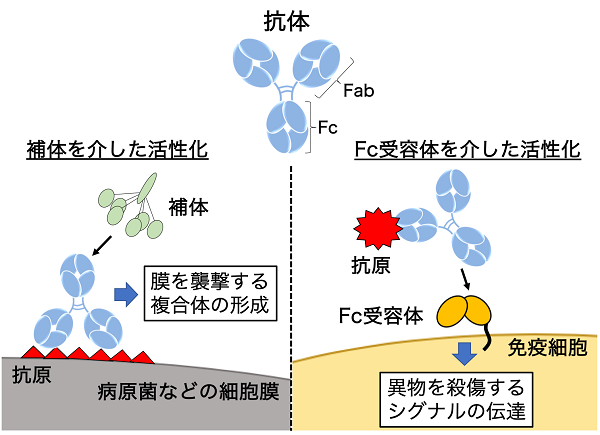
細菌やウイルスなどの異物が体内に侵入した際には、その異物を認識する抗体が私たちの体内で産生されますが、抗体が作り出されただけでは異物を排除することはできません。免疫細胞や血清中に存在する補体成分の助けが必要です。抗体はFab部分とFc部分からなり、Fab部分で抗原を認識し、Fc部分で免疫細胞や補体成分と結合すると考えられています。
抗体を介した免疫機能の発動経路は、補体成分を介した場合と免疫細胞を介した場合の大きく分けて2種類あります。補体成分を介した免疫機能が発動される際には、細菌やウイルスの表面にある抗原を認識した抗体に対して、血清中における補体成分が次々と誘導されることにより、最終的にウイルスなどの膜上に穴を開けることで殺傷します。
一方で、免疫細胞を介した免疫機能が発動される際には、抗原とくっついた抗体が免疫細胞上に存在する受容体と結合する必要があります。この結合をきっかけとして、免疫細胞内から異物を殺傷する成分が放出されます。
19世紀に北里柴三郎によって抗体の存在が発見されて以来、さまざまな生化学的手法を用いて、これらの分子機構の解明が試みられてきていますが、抗体の分子としての物理的性質の難しさから、その情報は断片的なものにとどまっています。
私たちは、高速原子間力顕微鏡という、分子レベルの小さな物質の動きをリアルタイムで観測することができる特殊な顕微鏡を用いることで、これまで捉えられていなかった抗体とその協力者の関わりあいを明らかにすることを目指しました。
抗体は「規則正しいリング構造」を作って補体成分と結合する
抗体が細菌やウイルスなどの表面にある抗原を認識すると、血清中における補体成分であるC1qが抗体にくっつきます。これを契機として、他の補体成分が次々とそこへ集まってきます。私たちは、「抗原を捉えた抗体にC1qが結合する」という一番最初のステップに着目し、高速原子間力顕微鏡を用いて抗体の振る舞いを観測することを試みました。
まず、細菌やウイルスの表面を模倣した抗原膜を作成し、この膜の上における抗体の振る舞いを観測しました。すると、驚くべきことに抗体は自発的に規則正しいリング構造を形成することが明らかとなりました。本来、抗体は単体で存在しますが、抗原膜上においては、抗体同士が規則正しく6つ集まっていたのです。

さらに、C1qを加えると、C1qは抗体のリング構造に対し、ちょうど真上に結合します。つまり、このリング構造はC1qが結合するうえで重要であり、補体成分による細菌やウイルスの膜を襲撃する複合体を形成するのにあたり、効率的であると考えられます。
抗原膜上の抗体のリング構造に対し結合するC1q
丸で囲った抗体のリング構造に対し、矢印で示したようにC1qが結合する様子を観測することに成功した。
これまで、抗体とC1qが結合するということはわかっていましたが、抗体単体とC1qの結合する強さはとても弱く、どのようにして他の補体成分が集まってくるのか明らかとなっていませんでした。しかし本研究により、抗体は抗原膜の上において、自発的に規則正しいリング構造を作ることで、C1qとの結合の強さを強め、効率的な膜襲撃体の形成が行われることが示唆されました。
抗体と受容体の新たな結合部位を発見
抗体が抗原を認識すると、免疫細胞の上にある受容体との結合を契機として免疫機能が発動されます。つまり、この抗体と受容体との結合が免疫機能の発動において非常に重要であると考えられます。抗体と免疫細胞の上にある受容体は、抗体のFc部分で結合すると考えられてきましたが、これまで得られている結合に関する情報は生体環境のものと大きく異なります。
そこで私たちはまず、溶液環境において抗体とFc受容体が結合する様子を高速原子間力顕微鏡で観測しました。すると、動画で示したように、抗体と受容体が結合する様子をリアルタイムで観測することに成功しました。
抗体とFc受容体が結合する様子
白い矢印で示したFc受容体に対し、ピンクの矢印で示した抗体が結合する様子を捉えることに成功した。
さらにFc受容体に対して抗体が結合している時間を観測すると、抗体は全長の方が強く結合することが明らかとなりました。これまで、その名のとおり、Fc受容体は抗体のFc部分と結合すると考えられていましたが、実は抗体のFab部分も結合に関わることが示唆されました。
そこで私たちはFab部分のどの部分が結合するのか、より詳細に理解するために、水素重水素質量分析法を用いて解析を行いました。すると下図に示す場所が結合に関わることが示唆されました。
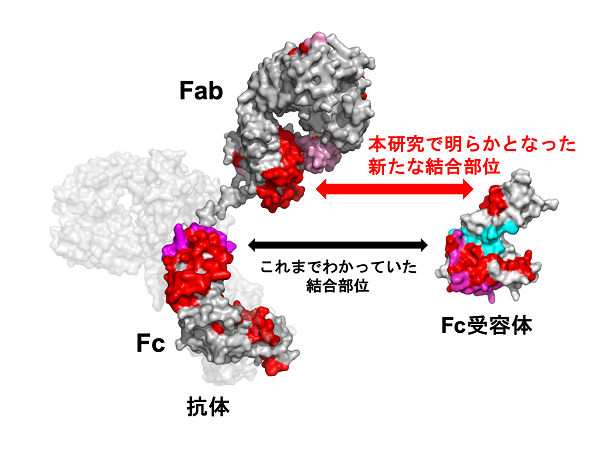
本結果により、これまで抗体はFc受容体に対し、Fc部分で結合すると考えられてきましたが、実はFab部分も受容体との結合に関与することが初めて明らかとなりました。
今後の展開
抗体は抗原に対する高い特異性と親和性から、がんの治療などを目的としたバイオ医薬品として広く使用されてきています。それらの多くは、上で説明したような、抗体と生体内に備わった免疫システムを利用したものです。一方、私たちの体の中で抗体の働きが暴走すると、ギラン・バレー症候群のような自己免疫疾患を引き起こしてしまうことも知られています。
本研究により、これまで見過ごされてきた抗体と免疫細胞、または抗体同士の新たな結合を明らかとすることで、さらに高い免疫機能を持ち合わせた抗体医薬品の開発や自己免疫疾患の治療につながることが期待されます。
参考文献
- Yanaka, S., Yogo, R., Watanabe, H., Taniguchi, Y., Satoh, T., Komura, N., Ando, H., Yagi, H., Yuki, N., Uchihashi, T. and Kato, K. “On-membrane dynamic interplay between anti-GM1 IgG antibodies and complement component C1q” Int. J. Mol. Sci. 21, 147, 2020
- Yogo, R., Yamaguchi, Y., Watanabe, H., Yagi, H., Satoh, T., Nakanishi, M., Onitsuka, M., Omasa, T., Shimada,M., Maruno,T., Torisu, T., Watanabe, S., Higo, D., Uchihashi, T., Yanaka, S., Uchiyama, S., and Kato, K. “The Fab portion of immunoglobulin G contributes to its binding to Fcγ receptor III” Sci Rep. 9(1):11957, 2019
この記事を書いた人

-
加藤 晃一(写真左)
自然科学研究機構生命創成探究センター(ExCELLS)センター長・教授。
1991年東京大学大学院薬学系研究科博士課程修了、薬学博士。名古屋市立大学薬学研究科教授兼務。日本核磁気共鳴学会会長。抗体の構造研究は大学院生のころから研究テーマです。現在、さまざまな分野の研究者と力をあわせて研究をする喜びを満喫しています。
與語 理那(写真右)
名古屋市立大学大学院薬学研究科 博士後期課程2年。日本学術振興会特別研究員。
現在は抗体の動的構造研究を通して、より高機能化した抗体の開発を目指しています。自分の研究がいつか医薬品として応用されることを夢見て研究に励んでいます。最近は合成生物学に興味があり日々勉強中です。