受精卵にDNAを入れると「人工細胞核」ができた!
細胞の中心「細胞核」
一般社会では、ものごとの中心になるものを「核」という言葉で表すことがあります。「核となる人」は中心人物のことですし、「核心をついた」という言葉は、“もっとも重要な部分”ということを意味します。細胞の中の「核」というのは、遺伝物質であるDNAを含んだ細胞小器官のことです。細胞が増殖したり活動したりするためには、DNAからRNAやタンパク質が作られる必要があります。そのため、細胞核は、細胞にとって生きていくのに欠くことができない最も重要な構造体ということができます。この重要な構造に「核」という言葉が充てられているのは、まさに「核心」をついたネーミングです。
細胞核は、細胞分裂時に崩壊し、再構築される
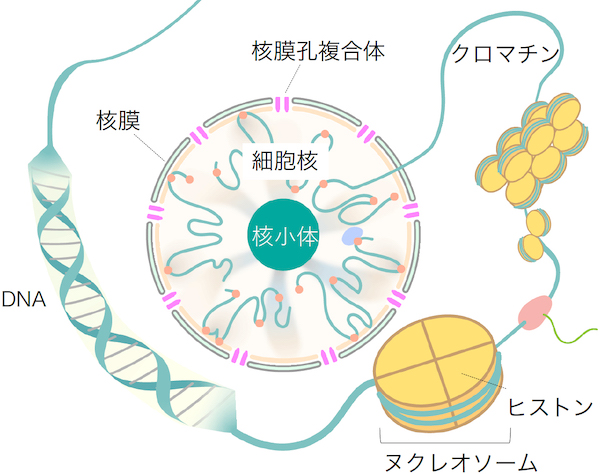
細胞核は、核膜という膜で覆われています。核膜は、2枚の膜が平行に重なった膜構造で、その2枚の膜をまたぐように多数の細かい孔が空いています。この孔は、1000個ぐらいのタンパク質が集まってできた構造で、核膜孔複合体と呼ばれています。核と細胞質間の物質のやり取りは、基本的に、この核膜孔複合体を通して行われます。核の内部には、DNAが存在しています。そのDNAには、146塩基対ごとにヒストンというタンパク質が結合していて、数珠の玉のような構造をとっています。この構造をヌクレオソームと呼びます。核内のDNAはヌクレオソームが数珠状に繋がった構造をとっています。この数珠状のDNAは、核膜の近くや、核小体の近くでは、さらに折りたたまれて凝縮した状態で存在しています。
細胞が増殖して分裂するとき、細胞核は崩壊し、再構築されます。しかし、このような精巧な構造体がいかにして毎回規則正しく形成され、機能性を獲得するようになるのか、その仕組みを担う要素を解析した報告はあまりありませんでした。
そのような要素を明らかにしようとして思いついたのが、特定の要素だけを細胞内に入れると、その部分に細胞核を構築することができるのではないかというアイデアです。つまり、人工的なビーズの表面に、調べたい要素となる因子(たとえば、DNAやタンパク質など)だけを結合させて、その周辺に核ができるかを調べれば、その要素が細胞核の構築にどのように重要かがわかります。
細胞核を人工的に造るには?
核を造るのに重要な要素として最初に調べたのはDNAです。DNAを微小なビーズ(磁気ビーズ)に結合させたDNAビーズを造って、細胞の中に入れ、ビーズに周りに細胞核ができるかどうかを調べました。サイズや素材など、どんなビーズを使うかいろいろと検討しました。そうして選んだのが約3μmの人工ビーズです。
約8 kbp(キロ塩基対)のDNAを結合させたDNAビーズを、ヒト子宮頸がん由来のがん細胞であるHeLa細胞に入れたところ、DNAビーズの周辺に核膜のような膜構造が形成されました。しかし、その核膜には、核膜孔複合体はありませんでした。したがって、細胞質から核内へタンパク質を運ぶ「核移行活性」もありませんでした。
この実験に用いたがん細胞は、体細胞です。つまり、体細胞の場合、DNAだけでは核膜の要素をすべて造ることはできないことがわかりました。さらに核膜孔複合体の因子のひとつを結合したビーズでも完全な核膜を構築することはできませんでした。
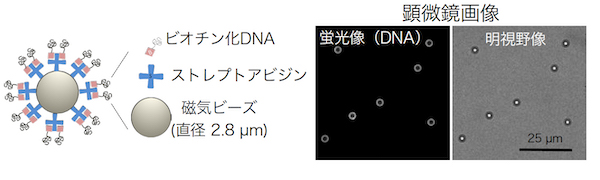
蛍光像の白い部分がDNA。 (「Suzuki et al., 2019」から転載)
そこで今回は、マウスの受精卵にDNAビーズを入れて、ビーズの周りに核ができるかどうかを調べました。核を造るためには、核膜やヒストンなどたくさんの成分が必要です。体細胞では、これらの成分についてせいぜい細胞2つ分の備蓄しかありませんが、受精卵は、たくさんの細胞を作り出すことができるので、たくさんの材料を備蓄しています。そこでDNAビーズを生きたマウスの受精卵の細胞質に導入し、ビーズの周辺に人工的な細胞核が構築される過程を生きたまま観察しました。
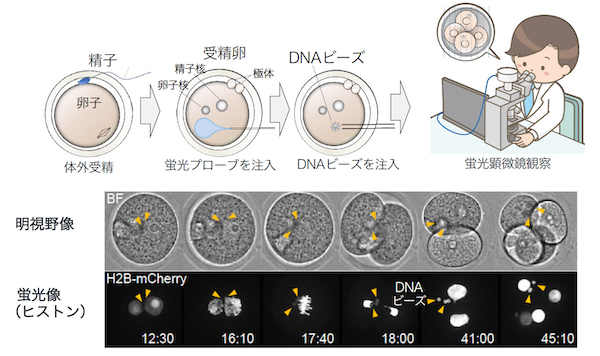
蛍光画像内の数字は「時間:分」。蛍光像の白い部分は、ヒストンH2Bタンパク質の挙動。矢頭は、DNAビーズの場所。 (「Suzuki et al., 2019」から改変して転載)
さらに、人工核を電子顕微鏡でも観察しました。その結果、DNAビーズ周囲にはヒストンが集積してヌクレオソーム構造が形成されるのに加え、核膜と核膜孔複合体がつくられて、かなり正常に近い核膜を持つ人工核様構造が構築されることがわかりました。しかしながら、残念なことに、体細胞の場合と同様、この「人工核」構造は、細胞質から核内へタンパク質を運ぶ「核移行活性」は持っておらず、その周囲には、タンパク質輸送に関わるRanタンパク質も存在しませんでした。このことから、受精卵といえども、核を造るためにはDNAだけでは足りず、他の成分が必要であることがわかりました。
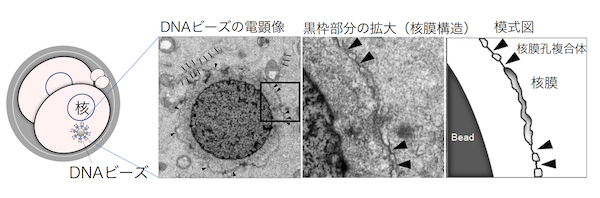
DNAビーズを入れたマウス卵の模式図(左)、DNAビーズ周辺の電子顕微鏡像(中央左はビーズ全体、中央右は拡大画像)、拡大画像の模式図(右)。矢頭は、核膜に形成された核膜孔複合体。(電顕像は「Suzuki et al., 2019」から転載)
驚いたことに、今回の実験では、DNAビーズを入れた受精卵は、生きたまま発生過程を観察しても正常に発生し、母親の子宮に戻すと仔マウスが産まれることを確認しました。DNAビーズは微小なもので、それが数個(~3個までは)入っていても発生にはまったく問題はありませんでした。
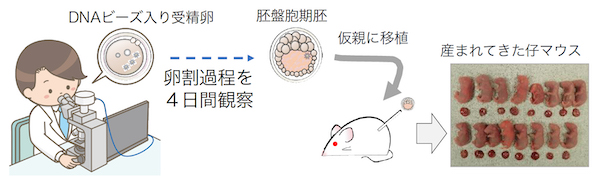
DNAビーズを導入した受精卵は、胚盤胞期胚期になるまで4日間、蛍光顕微鏡観察を行った後に、仮親に移植しても、仔マウスが得られた。 (写真は「Suzuki et al., 2019」から転載)
転写能のある人工核の構築を目指して
今回使ったDNAビーズでは、完全な働きをする人工核を造ることはできませんでした。しかし今後は、ビーズに結合させるDNAの配列や長さを変えたり、さらに特定のタンパク質を付加したりすることによって、受精卵の中で核移行活性をもつ人工核を造りだしたいと思います。そして、転写活性のある人工核を造ることが当面の目標です。それが実現すれば、核の構築に必要な因子について、より実効的な要素をあぶり出すことができます。さらに、もし人工核内で転写を起こさせることができたら、まったく新しいタイプの遺伝子治療法として発展させることが可能となります。
参考文献
- Suzuki Y, Bilir Ş, Hatano Y, Fukuda T, Mashiko D, Kobayashi S, Hiraoka Y, Haraguchi H, Yamagata K. Nuclear formation induced by DNA-conjugated beads in living fertilised mouse egg. Sci Rep, 2019 June 11; 9: 8461; doi.org/10.1038/s41598-019-44941-6.
- Bilir Ş, Kojidani T, Mori T, Osakada H, Kobayashi S, Koujin T, Hiraoka Y, Haraguchi T. (2019) Roles of Nup133, Nup153, and membrane fenestrations in assembly of the nuclear pore complex at the end of mitosis. Genes Cells, 2019 May; 24(5): 338-353. doi: 10.1111/gtc.12677. Epub 2019 Mar 22.
- Kobayashi S, Koujin T, Kojidani T, Osakada H, Mori C, Hiraoka Y, Haraguchi T. (2015). BAF is a cytosolic DNA sensor that leads to exogenous DNA avoiding autophagy. Proc Natl Acad Sci U S A. 2015 Jun 2; 112(22): 7027-32. doi: 10.1073/pnas.1501235112. Epub 2015 May 19.
この記事を書いた人

-
原口 徳子 (HARAGUCHI, Tokuko) 写真左
情報通信研究機構 主任研究員(1992年〜現在)。大阪大学大学院・理学研究科 招へい教授(1997〜現在)。大阪大学大学院・生命機能研究科 招へい教授(2007年〜現在)。細胞核構造と機能の解明を目指して研究を行っている。特に、細胞核機能を支える核膜構造をダイナミクスの観点から理解することを目指している。そのために必要なイメージング法の開発も行っている。蛍光イメージングと電子顕微鏡法を併用したLive CLEM(ライブ蛍光電子相関顕微鏡法)を開発した。
山縣 一夫 (YAMAGATA, Kazuo) 写真真ん中
1999年筑波大学農学研究科にて博士(農学)取得後、学術振興会特別研究員として大阪大学微生物病研究所に所属。その間、生化学的手法や遺伝子ノックアウト法により哺乳動物の受精に関わる分子の機能解析を行った。その後、筑波大学生命環境科学研究科講師、理化学研究所発生・再生科学総合研究センター研究員、大阪大学生体応答遺伝子解析センター特任准教授を経て、現職。その間、一貫して哺乳動物受精卵のライブセルイメージング技術の開発や、それによる生殖細胞・初期胚発生のクロマチン動態の定量解析を行ってきた。原口さんは僕にとってイメージングや細胞核の師匠である。
鈴木 由華 (SUZUKI, Yuka) 写真右
2019年近畿大学生物理工学部・生物理工学研究科(山縣一夫准教授のもと)にて修士号を取得。修士在籍時より、原口徳子教授との共同研究にて人工核再構成プロジェクトに取り組んできた。
この投稿者の最近の記事
 研究成果2019年9月2日受精卵にDNAを入れると「人工細胞核」ができた!
研究成果2019年9月2日受精卵にDNAを入れると「人工細胞核」ができた!



