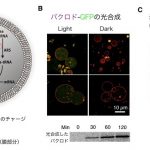
非生命から生命を作れるか? – 光からATPを生産してタンパク質を作る「人工細胞」の挑戦
「人工細胞」とは? – 細胞を”丸ごと”再構築する合成生物学の挑戦
合成生物学は、遺伝子や分子を人工的に組み合わせることで、生物システムを再構築し理解しようとする学問分野です。合成生物学では、生物システムをデザイン、操作、作製することを目的としています。なかでも、細胞を丸ごと人工的に組み立てようとする「人工細胞」の研究が、今世界的に進められており、日本の研究者はその大きなフラッグシップのひとつとして頑張っています。
なぜ人工細胞を作るのか? という質問をよく聞かれますが、その答え(学術的な意義)は、生命がシステムとして成立する仕組みや条件を完全に理解するためです。生物は非生物である分子や遺伝情報を組み合わせてできているので、何がどれくらい必要かがわかれば、理論的には人間が生物を作ることができるわけです。
もちろん、最初からヒト細胞のような高度な細胞は作れません。作れるのは、きっとラボの中の整えられた条件でやっと生きていける不完全な弱々しい細胞でしょう。しかし、そのような細胞は、地球上に初めて生命が誕生した当時の初期細胞と近似しているだろうという考えのもと、生命の起源研究にも大きな影響を与えています。最先端の合成生物学と、最もオールドスクールな生命の起源という学問分野が、今人工細胞を介して背中合わせになっているのはとてもおもしろい状況です。
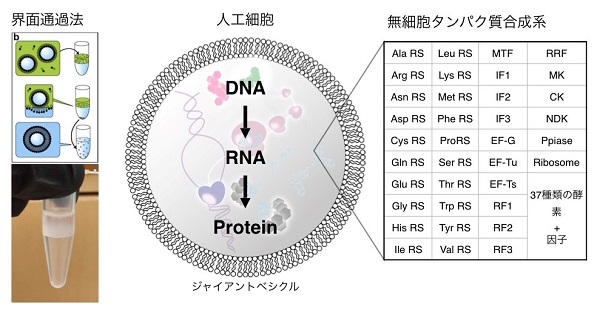
では、一体どうやって人工細胞を作るのか? 一言でいうと、膜という入れ物の中に必要な分子と遺伝子を閉じ込めて作ります。膜はリン脂質から作られ、リン脂質はある一定濃度以上あれば、その分子の性質から水の中で勝手にカプセル状の構造を作ります。今では界面通過法という方法で膜を作りますが、脂質を乾かして水和するフィルム水和法というやり方でも、膜を形成できます。
その膜の中に、DNAからタンパク質を合成するための酵素や因子をすべて入れ込めば、内部でタンパク質が合成されます。もちろんエネルギーも必要なので、ATPを一緒に加えておきます。しかし、当たり前ですが、ATPを使い切ってしまうと内部の反応は止まってしまいます。そのため、この人工細胞をより生物に近づけるためには、外部からのエネルギーを利用して、自分でエネルギーを生産する機能が必要になります。
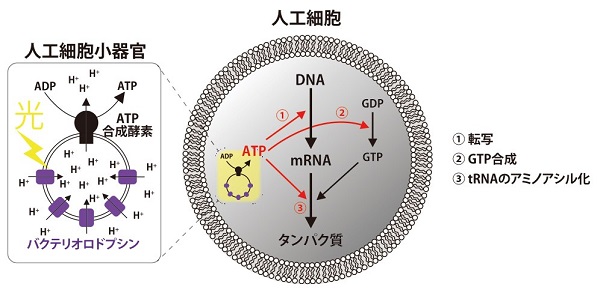
光からATPを合成する人工細胞小器官をつくるには?
実際の細胞の中のATPは一体どのように生産されるのかというと、それは膜上にあるATP合成酵素というタンパク質複合体により合成されます(解糖系からもATPが合成されますが効率は劣ります)。
しかし、水力発電の水車を回すために水の流れが必要なように、ATP合成酵素を駆動させるためのエネルギーも必要になります。膜の内外のプロトン濃度勾配がこれに当たります。細胞内では光合成反応や呼吸による電子伝達系によりプロトン勾配が形成されますが、これらは多くの因子から成る非常に複雑なシステムです。ということは、生物が長い進化の過程を経て獲得したシステムだと考えられます。
そのような複雑なシステムを獲得する前は、一体どうやって自律的にプロトン勾配を形成していたのでしょうか? 私たちはここでひとつの膜タンパク質に注目しました。「バクテリオロドプシン(以下、バクロド)」です。
バクロドは、光を当てると細胞内のプロトンを膜の外側に輸送する膜タンパク質で、ほぼ同じものが我々の目の中の網膜にたくさん存在します。バクロドは7回膜貫通型のタンパク質で、そのほとんどの部位が脂質膜の中に埋め込まれています。ちなみに、バクロドは世界で初めて構造解析された膜タンパク質です。このバクロドとATP合成酵素が同じ脂質膜のカプセル上にあれば、両者がコラボレートして、光エネルギーからATPが作れるというわけです。このときのカプセルは直径200nm程度の小さいもので構いません。
実は、このバクロドとATP合成酵素を組み合わせるアイデアは新しいものではありません。今から40年以上も前に吉田賢右先生らにより、バクロドとATP合成酵素を組み合わせてATP合成酵素の働きを観察したという論文が報告されています。
当時は単離したバクロドではなく、バクロドがたくさん存在するパープルメンブレンを使ったものでしたが、原理的には変わりません。この論文により、膜を介するプロトンの濃度勾配による膜電位差がATPを合成する直接のエネルギーである、という説が実験的に裏付けされました。
吉田先生はATP合成酵素の有名な研究者であり、この仕組みで人工細胞を作ろうというつもりはなかったと思いますが、その後同じアイデアを人工細胞のエネルギー生産系に利用しようとする論文がいくつか報告されました。しかし、合成されるATPのレベルが低いことなどから、残念ながら実装までには至りませんでした。
今回我々は、バクロドとATP合成酵素を組み合わせた人工細胞小器官の調製方法を工夫したこと、また逆回転を防ぐためにアジ化ナトリウムを利用したことで、効率のいい人工細胞小器官を作ることができました。この人工細胞小器官を細胞と同じくらいのサイズの膜(ジャイアントベシクル)にたくさん閉じ込めることで、ジャイアントベシクルの内部でもATPを作ることができます。定量してみると、1~3mMのATPが合成されていることがわかりました。これは生きた細胞内とほぼ同じレベルのATP濃度です。
世界で初めてジャイアントベシクル内部で光からATPを合成した、と言いたいところですが、残念ながら我々の報告の1年前に、韓国とアメリカのチームから論文が報告されました。このLeeらの研究では、同じような人工細胞小器官をジャイアントベシクルに閉じ込め、内部でATPを合成し、それによりアクチンフィラメントの重合や、炭素固定に成功しています。
この論文にはちょっとびっくりしましたが、これは細胞のような振る舞いを再現した研究であって、サステイナブルな細胞を作ろうとする我々の研究とは少しフォーカスが違うといえます。我々は、タンパク質合成のエネルギー源またはmRNA合成のための基質として、光合成されたATPを利用しようと研究を進めました。
光からタンパク質を合成する人工細胞
人工細胞内で光から生産したATPをエネルギー源としてタンパク質を合成するため、我々は人工細胞小器官と無細胞タンパク質合成系(以下、無細胞系)を組み合わせました。無細胞系は、試験管の中でDNAの持つ遺伝情報からタンパク質を合成するシステムのことで、この無細胞系をジャイアントベシクルの中に閉じ込めて反応させると、実際の細胞と同じようにタンパク質を作ることができます。
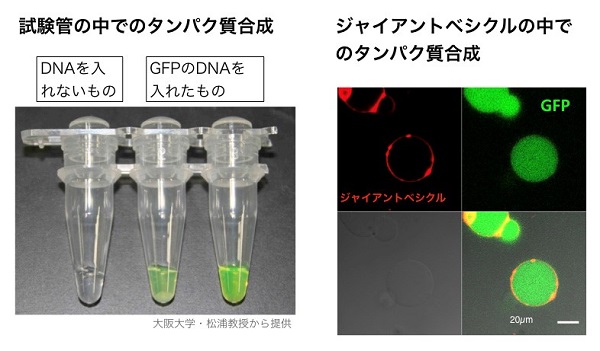
(右)ジャイアントベシクルの中でタンパク質を合成する人工細胞
多くの場合、無細胞系は大腸菌や小麦胚芽などの細胞抽出液をベースとして作ります。しかし、光合成したATPの効果を見るときに、すでに十分量のATPがもともとあったのでは、何を見ているのかわかりません。そのため、ATPが無い細胞抽出液を用意しなくてはなりませんが、ATPは細胞が生きるために必要な分子ですからこれは不可能です。また、細胞抽出液の中からATPだけを綺麗さっぱり取り除くことは技術的にほぼ無理といえます。
ではどうすればいいのか? そこで重要になってくるのが、「再構築型の無細胞系」です。再構築型の細胞系は、転写(DNAからmRNAを合成する反応)と翻訳(mRNAからタンパク質を合成する反応)に必要なすべての酵素を一つ一つ単離し、その他に必要となるtRNAやアミノ酸などと混ぜ合わせた、完全再構築型の無細胞系です。前者の抽出物系が体の一部を機械化したサイボーグだとたとえたら、再構築系の無細胞系はすべて人工物から作り上げたアンドロイドといえます。そのため、システムの中に何がどれくらい入っているのかをすべて把握することができるのです。
この再構築型の無細胞系はPURE systemと呼ばれ、2001年に清水義宏先生と上田卓也先生によって構築されました。つまりこのPURE systemを調製するときに、ATPを加えなければいいわけです。その代わりに、ATPの基になるADPを加えておきます。
このように調製したPURE systemと人工細胞小器官を組み合わせてジャイアントベシクルの中に閉じ込めて、光を当てながら温めました。すると内部で緑色に光るタンパク質(GFP)が合成されている様子が観察されました。人工細胞内で光エネルギーからタンパク質が合成された初めての結果です。
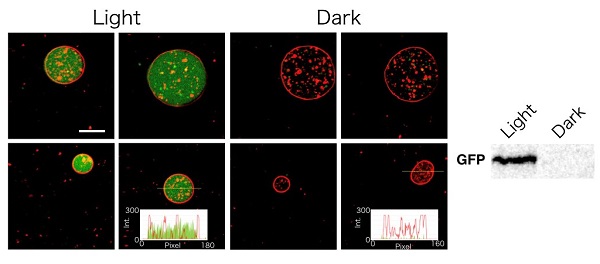
(右)合成されたタンパク質(GFP)のタンパク質電気泳動による可視化
自然光でもタンパク質を合成できるか?
光によりタンパク質を合成する実験は、人工細胞の入った反応溶液を温めつつ上から直接ランプの光を当てて反応を行います。しかし、この光は何もランプの光を使う必要はありません。太陽からの自然光でもいいわけです。
ちょうど実験を進めていた2018年の夏は天気が良く、また恐ろしく暑い時期でした。私たちはいつもどおり人工細胞を作ったあとラボの建物の屋上に持ち出し、水を貼ったタライに半日ほど浮かべておきました。その結果、ラボの中での実験と同じように、きちんとタンパク質が合成されていました。

これは、人工細胞が実際の環境中でも生存可能なことを暗示させる、我々にとってはたいへん意味のある実験でした。実際今の時点では反応がすぐに終わってしまう(死んでしまう)ため、危険はないものですが、研究が進むにつれて近いうちに厳密な研究ルールやガイドラインが必要になるかもしれません。
人工細胞が”自分で自分を作る”には?
光による人工細胞内でのタンパク質(GFP)合成の成功に浮かれつつも、私たちの目線は次の目標に移っていました。GFPはただ光るだけのタンパク質、といってしまえばそれまでです。他に機能を持ったタンパク質を作ってみたらどうなるでしょうか?
私たちは、人工細胞小器官のパーツであるバクロドのDNAを人工細胞に入れてみました。すると、人工細胞の中で合成されたバクロドが、内部の細胞小器官に埋め込まれたことを示す結果が得られました。もし正しく埋め込まれているのなら、細胞小器官1個あたりのバクロドの数が光合成する前よりも増えているはずです。つまりこれは、ATP合成酵素を駆動するためのエンジンが大きくなることを意味するので、エネルギー反応効率が上がっていると予想できます。
人工細胞の膜の中でこれを確かめることは難しいので、試験官の中で反応を行い人工細胞小器官の活性を比較してみました。その結果、光合成反応後にエネルギー反応効率が約1.5倍上がっていることが確認できました。
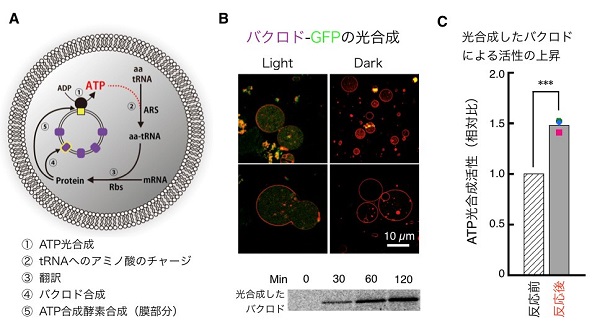
(B) バクロド – GFPの光合成
(C) 光合成したバクロドによるATP光合成活性の上昇
このことは、タンパク質により集められた光エネルギーからタンパク質が作られ、さらに光エネルギーを集めるという、正のフィードバックの仕組みができていることを意味します。また、同じ結果がもうひとつのパーツであるATP合成酵素の光合成(部分的)でもみられました。
この結果から、“人工細胞が光合成する”という研究視点から、“人工細胞が自分で自分を作る”という視点にシフトし、人工細胞はより一歩リアルな生物に進化することになりました。
人工細胞は自己複製できるか?
光という外部エネルギーからバクロドとATP合成酵素が合成されたことで、人工細胞が自己分裂した後も自ら細胞小器官を合成できることが、理論的に可能であると実証できました。しかし人工細胞は分裂し自己複製することが未だできません。これは人工細胞研究の一番のボトルネックになっています。
自己複製は生命が持つ最も重要な特徴です。近いうち人工細胞が内部の代謝を介して自己複製できるようになったとき、我々の生命システムに対する理解がより一層深まり、人工細胞が我々と同じく真に生きた細胞になるでしょう。その日はそう遠くないかもしれません。
参考文献
- Masasuke Yoshida, Nobuhito Sone, Hajime Hirata and Yasuo Kagawa, “ATP synthesis catalyzed by purified DCCD-sensitive ATPase incorporated into reconstituted purple membrane vesicles”, Biochem Biophys Res Commun. 67, 1295-1300 (1975).
- Keel Yong Lee, Sung-Jin Park, Keon Ah Lee, Se-Hwan Kim, Heeyeon Kim, Yasmine Meroz, L Mahadevan, Kwang-Hwan Jung, Tae Kyu Ahn, Kevin Kit Parker, and Kwanwoo Shin, “Photosynthetic artificial organelles sustain and control ATP-dependent reactions in a protocellular system”, Nat Biotech. 36, 530-535 (2018).
- Samuel Berhanu, Takuya Ueda, Yutetsu Kuruma, “Artificial photosynthetic cell producing energy for protein synthesis”, Nat Commun. 10, 1325 (2019).
この記事を書いた人

-
車 兪澈(くるま ゆうてつ)
海洋研究開発機構 研究員。東京大学大学院新領域創成科学研究科博士修了(生命科学)。イタリア・RomaTreでポスドク、東大院新領域・特任助教、東京工業大学地球生命研究所・特任准教授を経て、2019年より現職。合成生物学の分野で人工細胞を構築する研究に従事。生命現象を再構築すること生命の起源に迫ることを目指す研究にも取り組んでいる。